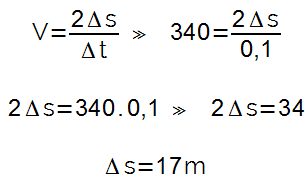numero di Massa (rappresentato dalla lettera A maiuscola) è la denominazione utilizzata per determinare la quantità protoni e neutroni presente all'interno del nucleo di qualsiasi atomo (rappresentato dalla sigla X).
Quando rappresentiamo il numero di Massa di qualsiasi atomo, il modo corretto di scriverlo è in alto a destra o a sinistra dell'abbreviazione dell'atomo, come possiamo vedere nello schema generale qui sotto:

Modelli di rappresentazione del numero di massa
Il numero di protoni in un atomo è dato da numero atomico (Z), che è sempre posizionato a sinistra dell'abbreviazione dell'atomo, in basso.
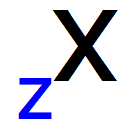
Rappresentazione del numero atomico nelle iniziali di qualsiasi atomo
come la numero di Massa indica sempre la quantità di protoni (p) e neutroni (n) all'interno del nucleo, è stata creata una formula basata su questa definizione:
A = p + n
Da questa espressione matematica, abbiamo la condizione per determinare:
Numero di Massa: in base al numero di protoni e al numero di neutroni;
numero di protoni: in base al numero di massa e al numero di neutroni, riscrivendo l'equazione come segue:
p = A - n
-
Numero di neutroni: in base al numero di massa e al numero di protoni, riscrivendo l'equazione come segue:
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
n = A - p
1° Esempio: Determinare il numero di neutroni presenti nel nucleo di un atomo di cloro, 17Cl35.
Nella dichiarazione, abbiamo due valori nell'acronimo, uno in basso a sinistra, che è il numero atomico o il numero di protoni, e un altro sopra, che è il numero di massa:
Z o p = 17
A = 35
Per determinare il numero di neutroni è sufficiente utilizzare i valori forniti nell'espressione utilizzata per calcolare la massa atomica, riscritti come segue:
n = A - p
n = 35 - 17
n=18
2° Esempio: Qual è il numero di protoni presenti all'interno del nucleo di un atomo di scandio, dato che il suo numero di massa e il numero di neutroni sono, rispettivamente, 43 e 21?
L'esercizio fornisce due valori, il numero di massa e il numero di neutroni. Presto:
A = 43
n = 21
Per determinare il numero di protoni è sufficiente utilizzare i valori forniti nell'espressione utilizzata per calcolare la massa atomica, riscritti come segue:
p = A - n
p = 43 - 21
p = 22
3° Esempio: Qual è il numero di massa di un atomo che ha un numero atomico pari a 60 e che ha 88 neutroni all'interno del suo nucleo?
L'esercizio fornisce due valori, il numero atomico (o il numero di protoni) e il numero di neutroni. Presto:
Z o p = 60
n = 88
Per determinare il numero di neutroni è sufficiente utilizzare i valori forniti nell'espressione utilizzata per calcolare il numero di Massa:
A = p + n
LA = 60 + 88
A = 148
Di Me. Diogo Lopes Dias
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
GIORNI, Diogo Lopes. "Cos'è il numero di massa?"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-numero-massa.htm. Consultato il 28 giugno 2021.