si definisce come ibridazione l'unione di orbitali atomici incompleti. Un orbitale è classificato come incompleto quando ne ha solo uno elettrone al suo interno invece di due. Guarda una rappresentazione di un orbitale incompleto e di un orbitale completo:

Nell'immagine A, abbiamo un orbitale completo; nell'immagine B, un orbitale incompleto.
L'ibridazione è un fenomeno naturale che si verifica con alcuni elementi chimici, come Fosforo, Zolfo, Carbonio, ecc. L'ibridazione del carbonio permette agli atomi di questo elemento di essere in grado di formare quattro legami chimici, cioè il carbonio fa solo quattro legami dopo aver subito il fenomeno dell'ibridazione.
Ma perché il carbonio si ibrida e forma quattro legami? Per comprendere questo fenomeno, dobbiamo conoscere la distribuzione elettronica di questo elemento:
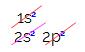
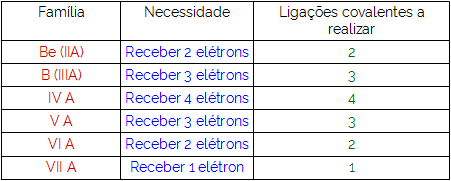
Nella distribuzione elettronica del carbonio, vediamo che il sottolivello 1s è completo (con due elettroni), il 2s è completo (con due elettroni) e il sottolivello 2p è incompleto (il sottolivello p supporta sei elettroni, ma c'è solo Due). Distribuendo gli elettroni 2p in modo rappresentativo, dobbiamo:
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
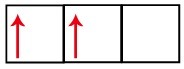
Il sottolivello p ha tre orbitali: nel caso del carbonio, due sono incompleti e uno è vuoto. Per questo motivo, questo elemento dovrebbe eseguire solo due collegamenti, poiché il numero di orbitali incompleti determina sempre il numero di collegamenti.
Tuttavia, quando si riceve energia dall'ambiente esterno, gli elettroni presenti nel carbonio vengono eccitati. Pertanto, uno degli elettroni presenti nel sottolivello 2s si sposta sull'orbitale del sottolivello p che era vuoto:
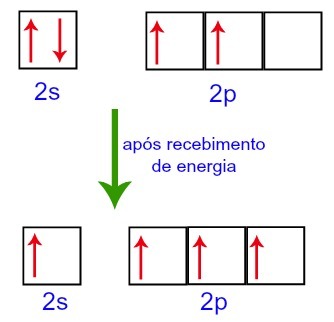
Orbitali di carbonio prima e dopo aver ricevuto energia dall'ambiente esterno
Pertanto, il carbonio rimane con quattro orbitali incompleti nel suo secondo livello. Quindi, l'orbitale di sottolivello 2s si unisce ai tre orbitali p, che configura il fenomeno di ibridazione.
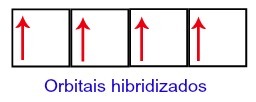
Orbitali di carbonio dopo l'ibridazione
Di Me. Diogo Lopes Dias
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
GIORNI, Diogo Lopes. "Ibridazione del carbonio"; Scuola Brasile. Disponibile in: https://brasilescola.uol.com.br/quimica/hibridizacao-carbono.htm. Consultato il 28 giugno 2021.