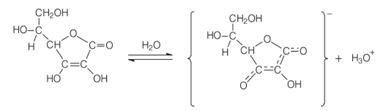
Il nome chimico di Vitamina C é acido L-ascorbico, o semplicemente Acido ascorbico. Questo nome trasmette i ruoli chimici e biologici di questo composto. L'aspetto chimico è che è acido, in quanto contiene nella sua struttura un gruppo fenolico-idrossi. Il gruppo fenolico attaccato al terzo carbonio della catena subisce ionizzazione in soluzione acquosa, come mostrato di seguito, rilasciando lo ione idrossido (H3oh+), che è caratteristico del comportamento acido:
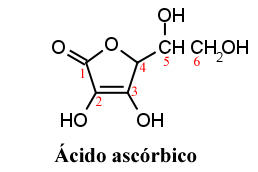
La parola “ascorbico” deriva dalla sua proprietà biologica di combattere la malattia chiamata scorbuto. E la "L" deriva dal fatto che l'acido ascorbico ha un centro asimmetrico al carbonio 5, con attività ottica. Tuttavia, la sua attività antiscorbuto deriva quasi interamente dall'isomero L (levogiro), che ha una rotazione specifica in acqua di 24°.
L'acido ascorbico fu isolato per la prima volta dal ricercatore ungherese Szent-Györgi nel 1922 come polvere cristallina bianca.
Gli esseri umani e altri animali come le scimmie, alcuni uccelli e alcuni pesci non sono in grado di sintetizzare la vitamina C. La carenza di questa vitamina nell'organismo porta alla sintesi difettosa del tessuto collagene e alla suddetta malattia, la
scorbuto.Tra i principali fonti di vitamina C, abbiamo frutta fresca, come ciliegia, anacardi, guava, ribes nero, mango, arancia, acerola, pomodoro, tra gli altri. Anche le patate sono un'ottima fonte di vitamina C, così come i peperoni e le verdure a foglia (bertalha, broccoli, cavoli, rape, foglie di manioca e patate dolci).

Diciamo "frutta fresco” perché la vitamina C può essere parzialmente o completamente distrutta durante lunghi periodi di conservazione. Ad esempio, ogni mese conservata, la patata perde il 15% della sua vitamina C. Inoltre, il calore può anche distruggerlo. I cibi cotti a lungo e quelli che hanno subito lavorazioni industriali contengono poca vitamina C. Nel caso delle patate, se cotte senza la buccia, perderanno immediatamente dal 30% al 50% delle sue proprietà.
Una delle principali proprietà dell'acido ascorbico è la sua capacità di agire come agente riducente. Poiché ha un'eccezionale facilità di ossidazione in soluzione acquosa, è un potente agente antiossidante, in quanto può ossidarsi al posto di altri composti.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Ad esempio, nella vita di tutti i giorni quando tagliamo certi frutti, come pere, banane e mele, con il tempo si scuriscono. Questo perché questi frutti contengono l'enzima polifenolo ossidasi, che provoca l'ossidazione enzimatica dei composti fenolici naturali in presenza di ossigeno molecolare, formando chinoni. Polimerizzano e generano melanine, che sono esattamente i pigmenti scuri e insolubili che vediamo formarsi in questi frutti.
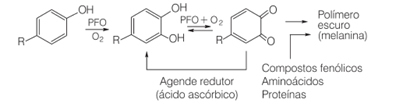
Uno dei modi per inibire l'azione dell'enzima polifenolo ossidasi è l'aggiunta di acido ascorbico. Questo avviene, ad esempio, quando aggiungiamo il succo d'arancia alla macedonia.
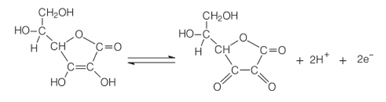
In presenza di ossigeno e di un catalizzatore, l'acido ascorbico si ossida, diventando il acido deidroascorbico. Questo acido ha un pH inferiore a 4 e un abbassamento del pH del tessuto del frutto fa rallentare la reazione di imbrunimento. A pH inferiore a 3, non vi è attività enzimatica.
Questa proprietà della vitamina C è ampiamente utilizzata in industria alimentare per prevenire la comparsa di sapore sgradevole, tossicità e per motivi economici, poiché stima che circa il 50% della perdita di frutti tropicali nel mondo sia dovuta all'enzima polifenolo ossidasi.
Per il suo ruolo antiossidante, la vitamina C è utilizzata anche in cosmetici. La sua applicazione topica attraverso questi cosmetici gli permette di raggiungere livelli che non sono possibili con la sola assunzione orale di vitamina C. Protegge la pelle dai raggi UV e dai radicali liberi che portano all'invecchiamento precoce.

di Jennifer Fogaça
Laureato in Chimica