Elektrolisis adalah proses yang banyak digunakan oleh industri kimia, karena memungkinkan untuk memperoleh zat yang tidak ada di alam bebas, seperti klorin, yodium, soda api, antara orang lain.
Elektrolisis adalah kebalikan dari sel, di mana listrik diperoleh melalui reaksi redoks, yaitu energi kimia diubah menjadi energi listrik. Sudah dalam elektrolisis, listrik digunakan untuk menghasilkan reaksi redoks dan energi kimia.
Karenanya asal usul namanya, karena itu elektro berarti "arus listrik" dan lisis berarti "pecah". Itulah yang terjadi, arus listrik memutuskan atau menguraikan zat yang dikenainya.
Baterai adalah proses spontan, elektrolisis, bagaimanapun, ini adalah proses yang tidak spontan, yang perlu dimulai dengan arus listrik.
Ada dua jenis elektrolisis: a berapi dan dalam media air. Dalam teks ini, kita akan berurusan dengan kasus pertama.
Perbedaan antara elektrolisis beku dan elektrolisis dalam media berair adalah bentuk zat yang akan dikenai arus listrik. Dalam kasus elektrolisis beku, zat ionik berada dalam keadaan cair, yaitu cair, tanpa adanya air.
Kata "berapi-api" berasal dari bahasa Latin berapi, yang berarti "membakar, meradang".Dalam elektrolisis digunakan wadah yang disebut a Kuba atau sel elektrolisis, di mana dua elektroda dipasang di mana arus listrik akan lewat. Elektroda dapat lembam (jangan berubah selama elektrolisis) atau aktif (Mereka mengalami semacam perubahan selama elektrolisis). Yang paling banyak digunakan adalah inert yang terbuat dari platinum atau grafit.
Elektroda kemudian dihubungkan ke sumber arus searah (sel atau baterai). Kutub negatif baterai akan mensuplai elektron ke salah satu elektroda, menjadi bermuatan negatif dan akan menarik kation (ion positif) dari zat cair. Karena menarik kation, elektroda negatif ini disebut katoda. Di dalamnya, kation menerima elektron dan mereduksi.
Elektroda positif menarik anion (ion negatif) dan, karena ini, disebut anoda. Anion melepaskan elektronnya di anoda, mengalami oksidasi.
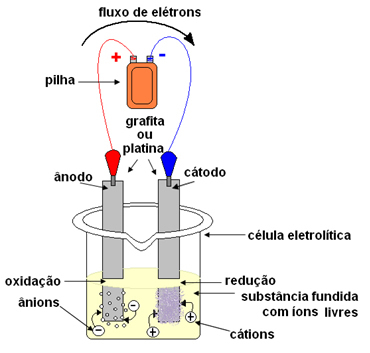
Pada baterai, elektroda positif disebut katoda dan elektroda negatif disebut anoda. Di sini dalam elektrolisis kebalikannya, anoda adalah kutub positif dan katoda adalah kutub negatif. Namun, dalam kedua kasus, dalam baterai dan elektrolisis, di anoda ada oksidasi dan di katoda ada reduksi.
Secara singkat, kami memiliki:

Fakta penting lainnya adalah bahwa sel atau baterai yang digunakan untuk menghasilkan arus listrik harus memiliki ddp (beda potensial) yang sama atau lebih besar dari perbedaan potensial reaksi.
Untuk lebih memahami bagaimana proses elektrolisis berlangsung dan bagaimana proses penguraian zat yang menghasilkan unsur penting atau zat sederhana, baca teks Elektrolisis Natrium Klorida Beku.
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/eletrolise-Ignea.htm


