Persamaan kimia dipahami sebagai deskripsi proses kimia, di mana reaktan dan produk yang berpartisipasi dalam reaksi ditunjukkan:
C + O2→ BERSAMA2
Reagen Produk
Agar ikatan kimia terjadi, harus ada pemutusan ikatan yang ada pada reaktan, dan pembentukan ikatan baru pada produk. Proses ini melibatkan studi tentang variasi energi reaksi.
Pasokan energi memungkinkan pemutusan ikatan reaktan (proses endotermik), sedangkan pembentukan ikatan dalam produk adalah proses eksotermik karena energi dilepaskan.
Energi ikat adalah yang dilepaskan dalam pembentukan produk dan secara numerik sama dengan energi yang diserap dalam pemutusan ikatan ini, sehingga energi ikat didefinisikan untuk pemutusan ikatan.
Ringkasnya: Energi ikatan adalah energi yang diserap untuk memutuskan 1 mol ikatan, dalam wujud gas, pada 25 °C dan 1 atm.
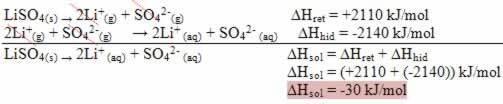
Lihat sekarang contoh bagaimana mendapatkan energi ikat reaksi:
HCl (g) → H (g) + Cl (g) H = + 103,0 Kkal/mol
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Persamaan di atas menunjukkan bahwa untuk memutuskan ikatan dalam 1 mol molekul HCl (g) dan membentuk 1 mol atom HCl H(g) dan 1 mol atom Cl (g), dibutuhkan 103,0 Kkal, yaitu energi ikat HCl (g) = + 103,0 Kkal/mol.
Stabilitas ikatan: semakin tinggi energi ikatan, semakin stabil ikatan. Contoh:
Jika energi ikat berikut diberikan:
H2O (1) → H2 (g) + O (g) H = + 110,6 Kkal/mol
HBr (g) → H (g) + Br (g) H = + 88,0 Kkal/mol
Apa yang akan menjadi tautan paling stabil, yang ada di HBr atau di H2HAI?
Energi ikat air (H2O) memiliki nilai lebih tinggi dari HBr, sehingga memiliki stabilitas yang lebih besar.
Oleh Liria Alves
Lulus kimia
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
SOUZA, Liria Alves de. "Energi Ikatan dalam Persamaan Kimia"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/energia-ligacao-equacoes-quimicas.htm. Diakses pada 28 Juni 2021.