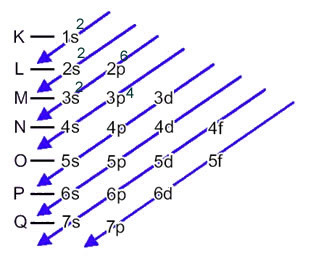
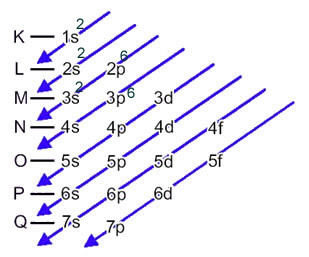
Distribusi elektron elektron atom dalam keadaan netral atau fundamental biasanya dilakukan dengan diagram pauling, ditunjukkan di bawah ini:
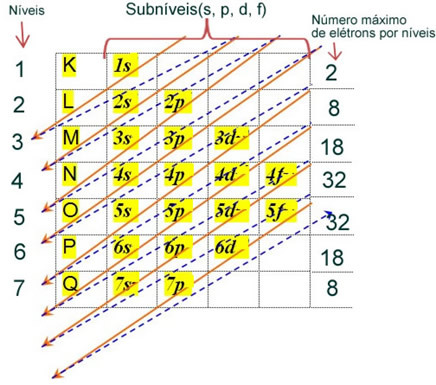
Aturan terperinci dari distribusi ini dapat ditemukan dalam dua teks berikut di situs web kami: “Distribusi elektron elektron" dan "Aturan Distribusi Elektronik”.
Distribusi elektronik ion awalnya bekerja dengan cara yang sama seperti atom dalam keadaan netral; dengan hanya satu perbedaan. Karena ion adalah atom yang telah memperoleh atau kehilangan elektron, kita harus memperhitungkan hal ini dan melakukan hal berikut:

Sebuah pengamatan penting adalah: perubahan dilakukan pada sublevel terluar dan bukan yang paling energik.
jika ionnya adalah kation, kita harus lepaskan elektron bahwa dia kalah. Mari kita lihat sebuah contoh:
Atom besi (nomor atom = 26) memiliki distribusi elektronik berikut di sublevel dalam urutan energik: 1 detik2 2 detik2 2p6 3 detik2 3p6 4s2 3d6. Adapun lapisan elektronik, kami memiliki: K =2; L = 8; M = 14; N = 2.
Distribusi ini ditunjukkan dalam diagram Pauling di bawah ini:
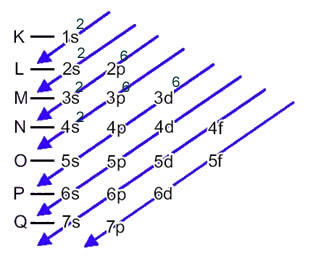
Ketika atom besi kehilangan 2 elektron, ia berubah menjadi kation Fe.2+. Jadi, saat membuat distribusi elektronik Anda, kami harus lepaskan 2 elektron dari kulit terakhir last(N) dan bukan dari sublevel yang paling energik, seperti yang ditunjukkan di bawah ini:
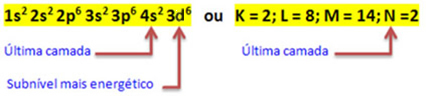
Jadi, distribusi elektron kation Fe Fe2+ diberikan oleh:
1 detik2 2 detik2 2p6 3 detik2 3p6 3d6 atau K = 2; L = 8; M = 14
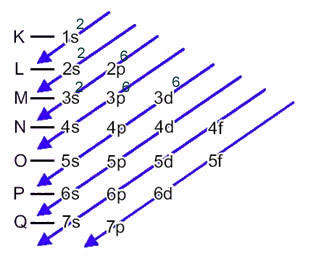
Sekarang, jika kita harus melakukan distribusi elektronik dari a anion, kita harus tambahkan elektron yang diterimanya.Lihat bagaimana ini dilakukan dalam contoh berikut:
Anion belerang (16s2-) terbentuk dari atom belerang (16S) dengan perolehan 2 elektron, seperti yang ditunjukkan oleh muatan 2-. Distribusi elektronik keadaan dasarnya diberikan oleh:
1 detik2 2 detik2 2p6 3 detik2 3p4 atau K = 2; L = 8; M = 6
Dalam hal ini, sublevel terakhir sama dengan sublevel energi, 3p. Jadi, kita tambahkan dua elektron dari anion belerang:
1 detik2 2 detik2 2p6 3 detik2 3p6 atau K = 2; L = 8; M = 8
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm


