ITU kelarutan, atau koefisien kelarutan, itu adalah sifat fisik materi yang selalu praktis ditentukan di laboratorium. Hal ini terkait dengan kapasitas suatu bahan, yang disebut zat terlarut, hadiah untuk dibubarkan oleh yang lain, the pelarut.
Adapun kelarutan, zat terlarut dapat diklasifikasikan sebagai berikut:
larut: yang larut dalam pelarut. Natrium klorida (zat terlarut), misalnya, larut dalam air (pelarut);
Sedikit larut: yang sulit larut dalam pelarut. Ini adalah kasus kalsium hidroksida [Ca(OH)2] (larutan) dalam air;
Tidak larut: yang tidak larut dalam pelarut. Pasir (zat terlarut), misalnya, tidak larut dalam air.
ITU kelarutan sangat terkait dengan persiapan solusi (campuran homogen), karena, untuk mendapatkan larutan, zat terlarut yang digunakan harus larut dalam pelarut.
Faktor-faktor yang mempengaruhi kelarutan
Bahkan ketika zat terlarut larut dalam pelarut, ada beberapa faktor yang dapat mempengaruhi kemampuan zat terlarut untuk larut. Apakah mereka:
a) Hubungan antara jumlah zat terlarut dan pelarut
Pelarut selalu memiliki batas zat terlarut yang dapat larut. Jika kita meningkatkan jumlah pelarut sambil mempertahankan jumlah zat terlarut, pelarut cenderung melarutkan semua zat terlarut yang digunakan.
B) Suhu
Suhu adalah satu-satunya faktor fisik yang mampu mengubah kelarutan pelarut terhadap zat terlarut tertentu. Modifikasi ini tergantung pada sifat zat terlarut, seperti yang akan kita lihat di bawah ini:
zat terlarut endotermik: adalah salah satu yang kami kelola untuk melarutkan massa yang lebih besar, selama pelarut berada pada suhu yang lebih tinggi dari suhu kamar. Semakin panas pelarut, semakin banyak zat terlarut akan larut.
Contoh: Dimungkinkan untuk melarutkan lebih banyak kopi bubuk saat air panas.
zat terlarut eksotermik: adalah salah satu yang kami berhasil melarutkan massa yang lebih besar, selama pelarut berada pada suhu lebih rendah dari suhu kamar. Semakin dingin pelarut, semakin banyak zat terlarut yang larut.
Contoh: Dimungkinkan untuk melarutkan lebih banyak karbon dioksida saat soda dingin.
Cara menentukan kelarutan
Karena kelarutan adalah sifat yang ditentukan dengan cara eksperimental, bahan, secara umum, telah dievaluasi kelarutannya dalam pelarut yang paling berbeda. Dengan demikian, kita dapat mengakses kelarutan zat terlarut dalam pelarut tertentu sebagai berikut:
a) Analisis tabel
Seringkali, siswa dapat menemukan kelarutan dari interpretasi tabel. Lihat contoh berikut:
Contoh: (UEPG - diadaptasi) Tabel di bawah menunjukkan kelarutan garam Li2BERSAMA3 dalam 100 gram air.

Tabel menyajikan nilai massa dalam gram Li2BERSAMA3 yang dapat dilarutkan dalam 100 gram air, dari 0 HAIC sampai 50 HAI. Kita dapat melihat bahwa semakin panas airnya, semakin sedikit Li2BERSAMA3 larut. Oleh karena itu, Li2BERSAMA3 itu adalah zat terlarut eksotermik (akan larut lebih banyak jika airnya dingin).
b) Analisis grafik
Kelarutan dapat dinilai dengan menafsirkan grafik. Untuk melakukan ini, cukup tentukan suhu, putar ke kurva dan kemudian putar kurva ke sumbu y, yang merupakan massa dalam gram zat terlarut yang akan dilarutkan.
Contoh: (UFTM - diadaptasi) Grafik menunjukkan kurva kelarutan garam AX2.
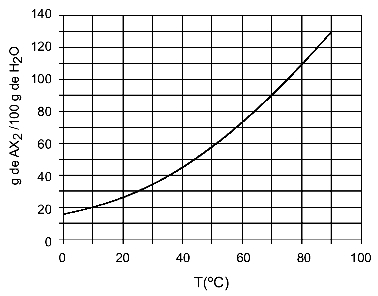
Grafik menyatakan bahwa, pada sumbu y, jumlah air (pelarut) adalah 100 gram. Untuk zat terlarut AX2, kita akan menentukan jumlah air pada suhu berikut:
30HAI: Saat kita menyalakan suhu 30HAIC ke kurva dan kemudian kurva ke sumbu y, kita memiliki bahwa, pada suhu ini, 100 gram air dapat melarutkan sekitar 35 gram zat terlarut AX2.
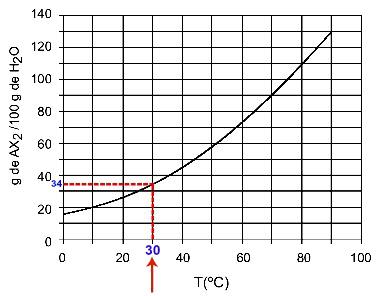
Penentuan kelarutan AX2 pada 30HAIÇ
40HAI: Saat kita menyalakan suhu 40HAIC ke kurva dan kemudian kurva ke sumbu y, kita memiliki bahwa, pada suhu ini, 100 gram air dapat melarutkan sekitar 45 gram zat terlarut AX2.
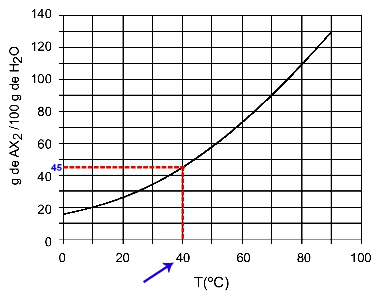
Penentuan kelarutan AX2 pada 40HAIÇ
Karena jumlah zat terlarut lebih besar dengan setiap kenaikan suhu, kita mendapatkan bahwa AX2 itu adalah zat terlarut endotermik.
c) interpretasi tekstual
Lihat contoh berikut:
Contoh: (PUC-MG) Zat tertentu mampu membentuk campuran homogen dengan zat lain. Zat yang jumlahnya paling banyak disebut pelarut dan zat yang jumlahnya paling sedikit disebut zat terlarut. Natrium klorida (NaCl) membentuk larutan homogen dengan air, di mana dimungkinkan untuk melarutkan, pada 20ClC, 36 g NaCl dalam 100 g air.
Teks tersebut menyatakan bahwa jika kita memiliki 100 gram air (pelarut), pada suhu 20 HAIC, dimungkinkan untuk melarutkan hingga 36 gram NaCl.
Oleh Saya Diogo Lopes Dias
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-solubilidade.htm


