Seperti yang dijelaskan dalam teks Reaksi Penambahan, reaksi organik ini biasanya terjadi dengan senyawa yang tidak jenuh (ikatan rangkap atau tiga kali lipat), di mana ikatan pi terputus, memungkinkan masuknya atom atau kelompok atom ke dalam rantai. karbonat.
Namun, jenis reaksi ini juga terjadi dalam kasus sikloalkana (hidrokarbon rantai tertutup dengan hanya ikatan jenuh (sederhana) antara karbon) yang memiliki tiga atau empat atom karbon. Perhatikan contoh di bawah ini, yang merupakan brominasi (reaksi halogenasi) dari siklopropana:
CH2
/ \ + br2 → br CH2 CH2 CH2 ─ br
H2C CH2
Demikian juga ada juga reaksi adisi yang disebut hidrohalogenasi atau adisi halida, seperti gambar di bawah ini:
CH2
/ \ + HBr → H CH2 CH2 CH2 ─ br
H2C CH2
Perhatikan bahwa, dalam kedua kasus, molekul itu rusak dan senyawa rantai terbuka diproduksi.
Tapi ini tidak terjadi dengan mudah pada sikloalkana dengan lima atau lebih atom karbon. Di sisi lain, senyawa ini lebih mungkin untuk melakukan reaksi substitusi, di mana ikatan tidak terputus, melainkan satu atau lebih atom hidrogen yang terikat pada karbon digantikan oleh atom unsur lain.
Siklopentana masih dapat melakukan reaksi adisi, tetapi hanya pada suhu yang lebih tinggi (sekitar 300 °C). Dalam kasus sikloheksana, ini sangat sulit. Apa yang sebenarnya dilakukannya adalah reaksi penggantian, seperti klorinasi berikut:
CH2 CH2
/ \ / \
H2C CH2 H2C CH Cl
│ │ + Cl2→ + HCl
H2C CH2 H2C CH2
\ / \ /
CH2 CH2
Cincin dengan lima atau lebih atom karbon tidak bereaksi dengan asam hidrohalat, seperti HBr, dalam reaksi adisi.
Tapi mengapa ini terjadi? Mengapa sikloalkana berkarbon tiga atau empat melakukan reaksi adisi dan sikloalkana dengan atom karbon lebih banyak cenderung tidak?
Nah, itu karena siklopropana dan siklobutana lebih tidak stabil, sehingga lebih mudah untuk memutuskan ikatannya.
Johann Friedrich Adolf von Bayer (1835-1917)
Untuk menjelaskan hal ini, ahli kimia Jerman Johann Friedrich Adolf von Bayer (1835-1917) mengembangkan, pada tahun 1885, apa yang disebut Teori tegangan cincin, yang menunjukkan bahwa empat ikatan yang dibuat oleh atom karbon akan lebih stabil ketika mereka memiliki sudut yang sama dengan 109º 28', seperti halnya dengan metana berikut:

Empat ikatan tunggal metana memiliki sudut 109º 28'
Ini adalah sudut yang paling stabil karena sesuai dengan kemungkinan jarak terbesar antara atom dalam geometri tetrahedral. Dengan ini, tolakan elektronik (penolakan antara elektron pada lapisan valensi atom) menjadi lebih kecil.
Sikloalkana dengan tiga, empat dan lima karbon memiliki sudut ikatan antara karbon kurang dari 109º 28'. Lihat:
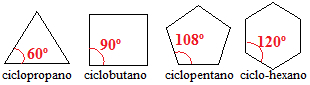
Sudut ikatan sikloalkana
Berdasarkan sudut nyata ini, yang secara umum dapat kita sebut, perhitungan tegangan ikat dapat dilakukan dengan menggunakan rumus berikut:
tegangan = 109º 28' - α
2
Kita tahu bahwa siklopropana adalah sikloalkana yang paling tidak stabil dan juga paling reaktif, dan ini dikonfirmasi dengan menghitung tegangan cincinnya dibandingkan dengan yang lain:
tegangan siklopropana = 109º 28' – 60º = 109º – 60º + 28' = 49º + 28' = 24,5º + 14
2 2 2
Sebagai 0,5º = 30, maka kita memiliki:
tegangan siklopropana = 24º + 30' + 14' = 24º 44'
tegangan siklobutana = 109º 28' – 90º = 9º 44'2
tegangan siklopentana = 109º 28' – 108º = 0º 44'2
Menurut teori tegangan Bayer, semakin besar tegangan ini, semakin tidak stabil siklon, yaitu, semakin besar perbedaan antara sudut nyata (α) dan sudut teoritis (109º 28'), lebih tidak stabil dan, akibatnya, lebih reaktif akan menjadi zat.
Itu sebabnya siklopropana adalah sikloalkana yang paling tidak stabil.
Namun, ada kesalahan dalam teori Bayer, karena jika kita terus melakukan perhitungan tegangan ini untuk sikloheksana, di mana sudut sambungan 120°, kita akan melihat bahwa nilainya akan lebih kecil dari siklopropana, memberikan sama dengan -5° 16'. Ini akan menunjukkan fakta bahwa sikloheksana seharusnya lebih tidak stabil dan melakukan reaksi adisi, yang dalam praktiknya tidak demikian.
Penjelasan untuk fakta ini ditemukan, pada tahun 1890, oleh ahli kimia Jerman Hermann Sachse dan dibuktikan, pada tahun 1918, oleh ahli kimia Jerman juga Ernst Mohr. Menurut para ilmuwan ini, kesalahan dalam teori tegangan cincin Bayer terletak pada kenyataan bahwa ia menganggap bahwa semua sikloalkana adalah koplanar, yaitu, semua atom karbonnya berada dalam satu bidang, bersamam gambar struktur mereka ditunjukkan di atas.
Namun, pada kenyataannya, cincin sikloalkana dengan lebih dari lima atom karbon tidaklah datar, melainkan atom-atomnya. memperoleh konformasi spasial yang membatalkan ketegangan antara sambungan, membentuk sudut 109º 28' antara Koneksi.
Misalnya, lihat kasus sikloheksana. Sebenarnya tidak datar dengan sudut 120° antara ikatannya, tetapi, pada kenyataannya, atom-atomnya "berputar", membentuk dua kemungkinan konformasi, konformasi "kursi" dan "perahu":
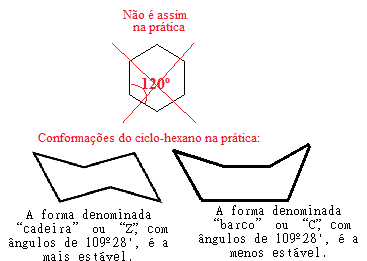
Kemungkinan konformasi sikloheksana dalam praktik
Perhatikan bahwa, karena sudut nyata sikloheksana sama dengan 109º 28', itu adalah senyawa yang sangat stabil, sehingga molekulnya tidak pecah, sehingga tidak berpartisipasi dalam reaksi adisi. Perhatikan juga bahwa bentuk "kursi" adalah yang paling stabil, karena selalu mendominasi dalam campuran, ini karena, dalam konformasi ini, atom hidrogen yang terikat pada karbon terpisah lebih jauh satu sama lain. orang lain.
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/teoria-das-tensoes-dos-aneis-bayer.htm