HAI muscovius, nomor atom 115, yang terletak di golongan 15 Tabel Periodik, merupakan salah satu unsur terakhir yang termasuk di dalamnya, pada tahun 2015, bersama dengan unsur 113, 117 dan 118. Namanya adalah referensi ke wilayah Moskow, ibu kota Rusia.
Moscovium, bagaimanapun, awalnya diproduksi, pada tahun 2003, melalui kerja sama ilmuwan Rusia dan Amerika. Meski begitu, hampir 20 tahun setelah sintesis awalnya, sifat dasarnya masih ditentukan. Jadi, banyak yang berspekulasi dan sedikit yang diketahui tentang sifat-sifatnya.
Tahu lebih banyak: Nama-nama unsur kimia baru — penghargaan untuk kota, wilayah, dan ilmuwan
abstrak tentang moscovius
Ini adalah unsur kimia sintetik yang terletak di kelompok 15 dari Tabel periodik.
Itu disintesis untuk pertama kalinya, pada tahun 2003, melalui kerja sama antara ilmuwan Rusia dan Amerika.
Itu membentuk kelompok unsur yang paling baru dimasukkan dalam Tabel Periodik, pada tahun 2015.
Studi mereka sangat baru, dengan sifat dasar masih ditentukan.
Produksinya dilakukan dengan fusi nuklir, menggunakan 48Ca dan atom-atom dari 243Saya.
properti Moskow
Simbol: Mc
Nomor atom: 115
Massa atom: 288 au.m.a (tidak resmi oleh Iupac)
Konfigurasi elektronik: [Rn] 7 detik2 5f14 6d10 7p3
Isotop paling stabil: 288Mc (waktu paruh 0,159 detik)
seri kimia: kelompok 15, elemen superberat
Fitur Muscovy
muscovius adalah salah satu elemen terakhir disertakanS dalam Tabel Periodik. Pencantumannya berlangsung pada 30 Desember 2015, dengan nama resminya dirilis pada 8 Juni 2016.
Sampai saat itu, unsur 115 dikenal dalam bahasa Portugis sebagai ununpentio, dari bahasa Latin, ununpentium, yang terjemahannya adalah “satu, satu, lima”. Nomenklatur lain yang diadopsi adalah eka-bismut, yang berarti "mirip dengan bismut", unsur periode keenam kelompok 15.
Muscovy adalah unsur sintetik, artinya hanya bisa diproduksi di laboratorium. Ini sangat umum di antara unsur-unsur superberat karena nukleusnya, dengan banyak proton dan neutron, tidak dapat distabilkan, sehingga tidak mungkin ditemukan di alam.
untuk menjadi elemen yang tidak stabil, itu dan elemen superberat lainnya akhirnya mengalami peluruhan radioaktif hampir seketika — emisi partikel elemen nuklir (seperti partikel α atau β) — dan transformasi yang diakibatkannya menjadi elemen lain yang lebih ringan, yang mungkin stabil atau TIDAK.
Berkenaan dengan itu, perlu dicatat bahwa studinya masih sangat baru, lagipula, kita menghadapi elemen yang diproduksi kurang dari 20 tahun yang lalu dan status resminya bahkan belum genap 10 tahun. Dalam hal ini, para ilmuwan lebih peduli dengan menentukan karakteristik dasar, seperti mereka massa atom dan perilaku kimianya dalam beberapa kemungkinan senyawa.
Misalnya, massa atom yang paling mungkin terdeteksi sejauh ini untuk otot adalah 288 unit massa atom. Belum lagi untuk mendapatkan muscovium sangat rumit, dengan a pendapatan hanya dari satu atom per hari.
Selain itu, atom yang dihasilkan tidak selalu dapat ditangkap untuk diukur massanya. Pada tahun 2018, para peneliti di Berkeley Laboratories, California, Amerika Serikat, hanya mampu mengukur satu massa per minggu. Dengan demikian, studi tentang sifat-sifat senyawanya masih dalam bidang kimia teori, dengan perhitungan dan model matematis untuk menentukan hasil yang diharapkan.
Mendapatkan Muscovy
Mendapatkan moscovium dilakukan dengan Fusi nuklir. ion dari 48Di Sini11+ (Z = 20) atom-atom yang dipercepat mengenai 243Am (Z = 95), disusun dalam bentuk AmO2 pada target melingkar titanium dari 32 cm², menghasilkan moscovium (Z = 115) dan tiga neutron.
Setelah tumbukan, sekitar satu mikrodetik (10-6 kedua), atom muscovy mengenai detektor, yang jaraknya sekitar empat meter dari lokasi tumbukan. Di jalur ini, elemen juga melewati pemisah, sehingga produk reaksi yang lebih ringan dialihkan. Di detektor, muscovium terdeteksi oleh pola peluruhan radioaktifnya.
Moscovium, sebagai atom radioaktif, mengalami peluruhan alfa (partikel radioaktif dengan dua proton dan dua neutron), sehingga menghasilkan unsur 113 (nihonium, Nh) menjadi unsur 105 (dubnium, Db). Akhirnya, Db berubah menjadi rutherfordium (Rf), yang terbagi menjadi dua fragmen dengan cepat. Pola peluruhan moscovium ditunjukkan di bawah ini.
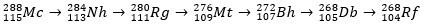
sejarah moskow
muscovius itu pertama kali disintesis pada tahun 2003, antara 14 Juli dan 10 Agustus, melalui kerja sama para ilmuwan dari Joint Institute untuk Riset Nuklir di Dubna, Rusia, dan Laboratorium Nasional Lawrence Livermore di Livermore, California.
Ion dari 48Ca sehingga mereka bisa bertabrakan dengan atom 243Am, awalnya menghasilkan isotop 291Mc. Selama proses tersebut, inti dipanaskan hingga 4 x 10 yang luar biasa11 K, dan kemudian didinginkan oleh emisi tiga neutron dan sinar gamma yang sangat cepat.

Tindakan ini membentuk isotop 288Mc. lalu moscovius dideteksi dan dianalisis berdasarkan pola peluruhan radioaktifnya (alfa meluruh). Nama Moskow adalah penghargaan untuk wilayah Moskow, Rusia.
Baca juga:Seaborgium — unsur kimia sintetik yang dinamai ilmuwan Glenn Seaborg
Latihan dipecahkan pada muscovius
pertanyaan 1
Moscovium, unsur yang baru ditemukan, ditempatkan di golongan 15 Tabel Periodik. Berdasarkan unsur lain dalam golongan ini, hidrida yang diharapkan untuk unsur ini adalah:
A) McH
B) McH2
C) McH3
D) McH4
E) Mc2H3
Resolusi:
Alternatif C
Unsur golongan 15 lainnya, seperti nitrogen Dia fosfor, sajikan rumus NH3 dan pH3 ketika terikat hidrogen. Dengan demikian, moscovium diharapkan menyajikan formula McH3 Juga.
pertanyaan 2
Pada tahun 2003, moscovium (Z = 115) disintesis untuk pertama kalinya, melalui kerja sama ilmuwan Rusia dan Amerika. Pada saat itu, isotop 288Mc terdeteksi dan produksinya penting untuk menempatkan unsur ini dalam Tabel Periodik. Jumlah neutron dalam isotop ini adalah:
A) 115
B) 288
C) 403
D) 173
E) 170
Resolusi:
Alternatif D
Jumlah neutron dapat dihitung seperti ini:
A = Z + n
Dimana A adalah nomor massa, Z adalah nomor atom, dan n adalah jumlah neutron. Mengganti nilai-nilai, kita mendapatkan:
288 = 115 + n
n = 288 – 115
n = 173
Oleh Stefano Araujo Novais
Guru kimia
