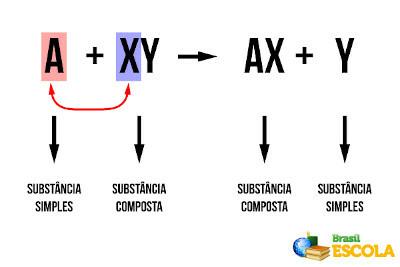
ITU baterai adalah sistem tempat berlangsungnya reaksi oksidasi-reduksi. Dalam perangkat ini, energi kimia yang dihasilkan dalam reaksi spontan diubah menjadi energi listrik.
Reaksi oksidasi dan reduksi terjadi secara bersamaan di dalam sel. Ketika satu spesies mengalami oksidasi, ia menyumbangkan elektron ke spesies lain, yang, setelah menerimanya, mengalami reduksi.
Oleh karena itu, yang mengalami oksidasi adalah zat pereduksi dan yang mengalami reduksi adalah zat pengoksidasi.
ITU oksidasi terjadi ketika suatu spesies kehilangan elektron dan menjadi kation: A → A+ + dan-.
ITU pengurangan terjadi ketika suatu spesies memperoleh elektron dan menjadi netral secara listrik: B+ + dan- → B
Dalam persamaan kimia, ini transfer elektron ditunjukkan oleh perubahan bilangan oksidasi (nox).
Reaksi reduksi terjadi di dalam sel dan arus listrik muncul dengan migrasi elektron dari kutub negatif ke kutub positif.

Bagaimana cara kerja tumpukan?
Satu reaksi redoks umumnya dapat diwakili oleh persamaan:
A + B+ → A+ + B
Di mana,
A: zat yang teroksidasi, kehilangan elektron, meningkatkan nilainya dan merupakan agen pereduksi.
B: zat yang mengalami reduksi, memperoleh elektron, menurunkan oksidasi dan merupakan oksidator.
Lihat pada gambar berikut bagaimana proses ini dapat direpresentasikan.
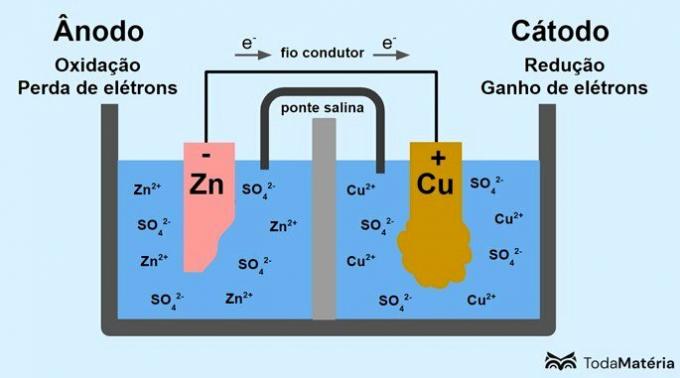
Sistem yang dibagi menjadi dua semisel dan dibentuk oleh dua elektroda logam yang dihubungkan secara eksternal oleh kawat penghantar dikembangkan oleh John Frederic Daniell (1790-1845) pada tahun 1836.
Baterai terdiri dari dua elektroda, dihubungkan oleh kawat penghantar, dan elektrolit, di mana ion berada. Elektroda adalah permukaan konduktor padat yang memungkinkan pertukaran elektron.
anoda: elektroda tempat terjadinya oksidasi. Ini juga merupakan kutub negatif baterai.
Katoda: elektroda di mana reduksi terjadi. Ini juga merupakan kutub positif baterai.
Pada gambar di atas, seng logam adalah anoda dan mengalami oksidasi. Tembaga logam adalah katoda dan mengalami reduksi. Perpindahan elektron (e-) terjadi dari anoda ke katoda melalui kawat penghantar.
Reaksi yang terjadi pada sistem citra adalah:
- anoda (oksidasi): Zn(s) → Zn2(di sini) + 2e-
- Katoda (pengurangan): Cu2+(di sini) + 2e- → keledai(s)
- persamaan umum: Zn(s) + pantat2+(di sini) → keledai(s) + Zn2+(di sini)
Seng adalah logam dengan kecenderungan lebih besar untuk kehilangan elektron dan, oleh karena itu, kation terbentuk dalam larutan. Elektroda seng mulai aus dan kehilangan massa karena seng dilepaskan ke dalam larutan saat membentuk kation Zn2+.
Elektron dari anoda tiba di katoda dan kation logam, setelah menerimanya, diubah menjadi tembaga logam, yang disimpan pada elektroda dan meningkatkan massanya.
Jembatan garam adalah arus ionik yang bertanggung jawab untuk sirkulasi ion dalam sistem agar tetap netral secara elektrik.
Baca juga tentang bilangan oksidasi (nox).
jenis baterai
Dalam sel, kecenderungan spesies kimia untuk menerima atau menyumbangkan elektron ditentukan oleh potensial reduksi.
Komponen dengan potensial reduksi tertinggi cenderung mengalami reduksi, yaitu memperoleh elektron. Spesies dengan potensial reduksi terendah dan, akibatnya, potensial oksidasi tertinggi, cenderung mentransfer elektron.
Misalnya, dalam reaksi redoks Zn0(s) + pantat2+(di sini) → keledai0(s) + Zn2+(di sini)
Seng mengoksidasi dan mendonorkan elektron karena memiliki potensial reduksi E0 = -0,76V, lebih kecil dari potensial reduksi tembaga E0 = +0,34V dan, oleh karena itu, menerima elektron dan mengalami reduksi.
Lihat di bawah untuk contoh tumpukan lainnya.
Tumpukan seng dan hidrogen
Setengah reaksi oksidasi: Zn(s) → Zn2+ + 2e- (DAN0 = -0,76V)
Setengah reaksi reduksi: 2H+(di sini) + 2e- → H2 (g) (DAN0 =0,00V)
Persamaan global: Zn(s) + 2H+(di sini) → Zn2+(di sini) + H2 (g)
Representasi tumpukan:
Sel tembaga dan hidrogen
Setengah reaksi oksidasi: H2 (g) → 2H+(di sini) + 2e- (DAN0 = 0.00V)
Setengah reaksi reduksi: Cu2+(di sini) + 2e- → keledai(s) (DAN0 = +0,34V)
Persamaan Global: Cu2+(di sini) + H2 (g) → 2H+(di sini) + pantat(s)
Representasi tumpukan:
Dapatkan lebih banyak pengetahuan tentang topik dengan konten:
- elektrokimia
- Elektrolisa
Referensi bibliografi
FONSECA, M. R. M. Kimia, 2. 1. ed. Sao Paulo: Attica, 2013.
SANTOS, W.L.P; MOL, G.S. Kimia warga, 3. 2. ed. Sao Paulo: Editora AJS, 2013.
USBERCO, J. Hubungkan kimia, 2: kimia. - 2. ed. Sao Paulo: Saraiva, 2014.