Semakin tinggi suhu, semakin besar kecepatan reaksi.
Ini dapat dengan mudah dilihat dalam banyak situasi dalam kehidupan kita sehari-hari, seperti dalam contoh berikut:
- Ketika kita ingin memperlambat reaksi dekomposisi makanan, kita menurunkan suhu, menempatkannya di lemari es;

- Jika kita ingin mempercepat reaksi memasak makanan, masukkan saja ke dalam panci masak. tekanan yang, dengan meningkatnya tekanan, juga meningkatkan suhu didih air cair di mana makanan adalah;

- Kebakaran, pada umumnya, biasanya merusak karena suhu lingkungan meningkat, yang menyebabkan peningkatan kecepatan reaksi pembakaran;
- Untuk memperlambat proses kimia metabolisme, mengurangi kemungkinan kerusakan otak karena kekurangan oksigen, beberapa operasi dilakukan dengan menurunkan suhu tubuh pasien, mencapai sekitar 15°C;
- Jika kita memasukkan tablet effervescent ke dalam segelas air panas dan satu lagi ke dalam segelas air dingin, yang pertama akan larut lebih cepat.
Tapi apa yang menjelaskan pengaruh proporsional langsung dari suhu pada laju reaksi?
Ini karena, seperti yang dijelaskan dalam teks “Kondisi Terjadinya Reaksi Kimia”, agar reaksi dapat berlangsung, perlu memenuhi beberapa kondisi, seperti partikel mereka harus bertabrakan secara efektif dan dengan energi minimum yang diperlukan, yang disebut energi aktivasi.
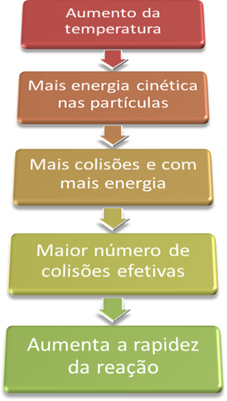
Jadi, ketika kita meningkatkan suhu sistem, kita juga meningkatkan agitasi partikel yang bereaksi dan memberi mereka lebih banyak energi kinetik. Dengan ini, lebih banyak tumbukan akan terjadi dan dengan lebih banyak energi, meningkatkan jumlah partikel yang akan bereaksi dan, akibatnya, meningkatkan kecepatan reaksi.
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/temperatura-velocidade-das-reacoes.htm

