Polimerisasi adalah nama proses kimia yang menghasilkan pembentukan makromolekul (molekul besar) yang disebut polimer, melalui kombinasi molekul yang lebih kecil, monomer.
reaksi dari polimerisasi itu sangat umum di alam, seperti yang dapat kita lihat pada karbohidrat (seperti pati) dan protein (seperti kasein dalam susu). Ini juga terjadi secara sintetis, karena sebagian besar polimer yang digunakan oleh manusia dalam kehidupan sehari-hari dibuat secara artifisial.
Polimer pertama yang dihasilkan dari polimerisasi sintetis adalah Bakelite, pada tahun 1909, oleh ahli kimia Belgia Leo Hendrik Baekeland.
Secara umum, untuk monomer yang akan digabungkan dengan yang lain (apakah mereka sama atau berbeda) dalam reaksi polimerisasi, diperlukan adanya valensi bebas (ikatan kimia yang akan dilakukan) pada kedua monomer tersebut.
Valensi ini timbul sebagai akibat dari pemutusan ikatan, melalui penggunaan katalis (seperti nikel), kondisi eksternal seperti cahaya dan panas, atau oleh fenomena resonansi dalam struktur (pergeseran elektron).
Dalam pembentukan polipropilen (polimer PP), misalnya, digunakan dalam peralatan rumah tangga dan mainan, tautan pi (π) dalam setiap molekul dipecah sebagai berikut:
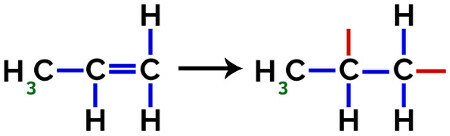
Putusnya ikatan pi dalam propilena
Dengan demikian, setiap monomer propilena dapat berikatan dengan dua monomer propilena lainnya dan membentuk polimer PP atau polipropilena (awalan poli menunjukkan beberapa unit monomer). Cara yang paling sering untuk menyatakan suatu polimer adalah dengan monomer di antara tanda kurung dan, di luar, huruf n, yang menunjukkan beberapa monomer, seperti yang dapat kita lihat dalam kasus polimer PP:
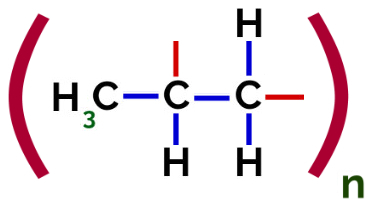
Representasi polimer PP
reaksi dari polimerisasi dapat dilakukan dengan berbagai cara, seperti yang akan kita lihat di bawah ini:
a) Reaksi dari penambahan polimerisasi
Di dalam polimerisasi, selalu ada pemutusan ikatan pi dalam monomer, yang menyebabkan dua valensi bebas muncul dalam struktur, seperti dalam pembentukan polietilena, polimer banyak digunakan dalam kemasan farmasi.
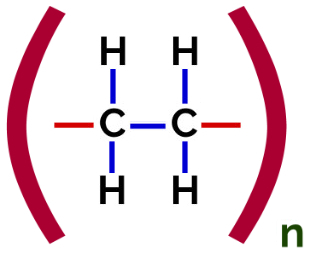
Formula Struktur Polimer Penambahan Polietilen
Pada polimerisasi dari polietilen, molekul etilen (etena), yang memiliki ikatan pi antara dua atom karbon, digunakan sebagai monomer. Ketika ikatan ini diputus, dua valensi bebas muncul, satu pada setiap atom karbon yang terlibat dalam ikatan pi. Monomer bersatu persis di masing-masing valensi ini, yaitu, valensi satu terkait dengan valensi yang lain, dan seterusnya.
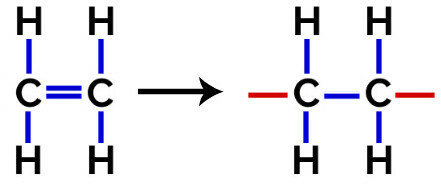
Persamaan Pembentukan Polietilen
b) Reaksi polimerisasi adisi 1.4
Dalam polimerisasi ini, monomer menghadirkan dua ikatan rangkap bolak-balik (satu pi dan satu sigma), yang mendukung fenomena tersebut. resonansi (mengganti posisi elektron pi dari ikatan pi), seperti dalam pembentukan karet sintetis (polibutadiena)

Rumus struktur polibutadiena
Unit monomer dari polimer ini adalah butadiena, yang memiliki dua ikatan rangkap yang berselang-seling. Dengan resonansi, struktur memiliki ikatan rangkap antara karbon 2 dan 3, dan dua valensi bebas pada karbon 1 dan 4. Justru dalam valensi bebas karbon 1 dan 4 inilah monomer bergabung.

Resonansi butadiena
c) Reaksi dari polimerisasi kondensasi atau eliminasi
Ini adalah reaksi dari polimerisasi di mana, wajib, dua monomer (sama atau berbeda) secara bersamaan kehilangan atom atau kelompok, menghasilkan dua valensi bebas di masing-masing dari mereka. Dengan cara ini, selalu ada eliminasi hidrogen dari monomer, yang kemudian bergabung dengan halogen (F, Cl, Br, I), OH, NH2, atau ke CN monomer lainnya.
Jadi, di polimerisasi dengan eliminasi, selalu ada pembentukan air, asam halogenasi (HCl, HI, HF, HBr), amonia (NH3) atau asam hidrosianat (HCN) di samping polimer. Lihat, misalnya, representasi pembentukan poliester, bahan yang digunakan sebagai kain:

Persamaan Pembentukan Poliester
Monomer pembentuk poliester adalah asam p-benzenadioat dan etana-1,2-diol. Kita dapat mengamati bahwa dalam hal ini polimerisasi penghapusan molekul air terjadi, karena dua monomer memiliki dua hidroksil. Dalam proses ini, asam kehilangan dua hidroksil, dan dialkohol hanya kehilangan hidrogen dari hidroksilnya:

Struktur Poliester
Monomer poliester bergabung dengan oksigen dalam alkohol dan karbon dalam asam karboksil.
Oleh Saya Diogo Lopes Dias
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm
