Oksidasi adalah nama yang diberikan untuk proses hilangnya elektron oleh atom, kelompok atau spesies ionik selama a reaksi kimia. Hal ini diketahui dari peningkatan NOX (bilangan oksidasi) dari spesies atau atom ketika membandingkan reaktan dan produk.
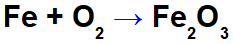
Persamaan oksidasi besi.
Dalam persamaan di atas, misalnya, kita dapat menunjukkan NOX dari masing-masing peserta:
Reagen besi (Fe): memiliki NOX 0 seperti a bahan sederhana;
Oksigen dalam reagen (O): memiliki NOX 0 karena merupakan zat sederhana;
Oksigen dalam produk: memiliki NOX -2 karena tidak terkait dengan logam alkali, alkali tanah atau pembentukan hidrogen peroksida atau superoksida;
Besi dalam produk: memiliki NOX +3 karena jumlah NOX besi dikalikan 2 (jumlah atom) + NOX oksigen dikalikan 3 harus menghasilkan 0 karena merupakan zat majemuk:
x.2 + 3.(-2) = 0
2x - 6 = 0
2x = +6
x = + 6
2
x = +3
Membandingkan NOX besi reagen (0) dengan produk (+3), kami mengamati peningkatan, yaitu, mengalami proses oksidasi. Perlu dicatat bahwa terjadinya oksidasi
itu selalu disertai dengan fenomena reduksi (yang berarti perolehan elektron), yang diidentifikasi dengan penurunan NOx, seperti yang terjadi pada oksigen dalam contoh.Baca juga:Penentuan Bilangan Oksidasi (NOX)
Contoh situasi di mana oksidasi terjadi:
1. Pembakaran

Pembakaran suatu bahan juga merupakan indikasi oksidasi.
Pembakaran adalah setiap reaksi kimia yang terjadi dengan adanya bahan bakar apapun dan gas oksigen pengoksidasi (O2), menghasilkan produksi panas dan cahaya. Dalam setiap reaksi pembakaran terjadi oksidasi.
2. Beberapa reaksi organik
Dalam setiap reaksi organik yang terjadi dengan adanya sarana yang tercantum di bawah ini, proses oksidasi:
Kalium dikromat (K2Cr2HAI7) atau kalium permanganat (KMnO4);
Adanya asam kuat atau basa kuat;
Gas ozon (O3) dengan adanya logam seng (Zn) dan air (H2HAI).
3. Baterai atau baterai

Baterai adalah perangkat di mana oksidasi selalu terjadi.
Tumpukan atau baterai adalah perangkat elektrokimia yang menyimpan zat kimia. Salah satu zat ini akan mengalami oksidasi, dan yang lainnya akan mengalami reduksi, sehingga menghasilkan arus listrik.
4. Elektrolisa
Elektrolisa adalah proses kimia di mana larutan berair yang mengandung garam dikenai arus listrik, yang akhirnya mendorong oksidasi anion yang ada dalam bahan ini. Dalam semua elektrolisis, ada oksidasi.
Oleh Saya Diogo Lopes Dias
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-oxidacao.htm

