Mekanisme adalah simulasi cara reaksi diproses, menggambarkan langkah-langkah yang dilalui reaktan untuk mencapai produk akhir.
Mekanisme diusulkan berdasarkan percobaan, karena tidak mungkin untuk memvisualisasikan langkah demi langkah reaksi, dan sangat berguna dalam Kimia Organik, karena senyawa organik bereaksi satu sama lain dalam berbagai cara: memutuskan ikatan, membentuk senyawa perantara.
Ada faktor-faktor yang mengganggu produk akhir reaksi, seperti, misalnya, sifat pelarut, polaritas ikatan, pertukaran elektron, dll. Oleh karena itu, mekanisme tertentu tidak selalu merupakan satu-satunya cara untuk pembentukan produk, mereka dapat terjadi dengan cara yang berbeda, secara ionik atau melalui radikal bebas, misalnya.
1. mekanisme ionik: proses yang dimulai melalui pemutusan ikatan kovalen secara heterolitik dan pembentukan ion (karbokation dan karbanion).
Lacak Mekanisme Halogenasi Alkena.
Kami dapat membagi mekanisme menjadi beberapa tahap:
Tahap 1: Gangguan heterolitik pada ikatan kovalen (Cl – Cl): pembentukan karbokation dan anion (Cl-).
Tahap 2: Serangan anion klorida (Cl-) pada karbokation.
Tahap 3: Pembentukan produk 1,2 - dikloropropana.
Seperti dapat dilihat, Halogenasi Alkena terjadi melalui mekanisme ionik.
Catatan: Sesuai namanya, Halogenasi dilakukan dengan menambahkan Halogen (Klorin) ke dalam molekul.
2. Mekanisme melalui radikal bebas: pemutusan ikatan kovalen homolitik membentuk radikal bebas (sangat tidak stabil dan reaktif), mari kita lihat contohnya:
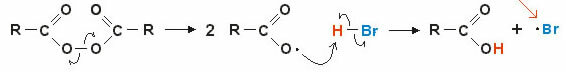
Reaksi dimulai dengan pemutusan ikatan peroksida dan pembentukan radikal bebas. Pada tahap antara, serangan radikal terjadi pada hidrogen terpolarisasi (H — Br) dan akibatnya membentuk radikal bebas baru • br (sangat tidak stabil dan reaktif).
Oleh Liria Alves
Lulus kimia
Tim Sekolah Brasil
Lihat lebih banyak!
Radikal dalam Kimia Organik
Kimia organik - Kimia - Sekolah Brasil
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/quimica/mecanismos-reacoes-organicas.htm
