HAI keseimbangan persamaan memungkinkan kita untuk mencocokkan jumlah atom yang ada dalam persamaan kimia sehingga menjadi benar dan mewakili reaksi kimia.
Gunakan pertanyaan di bawah ini untuk menguji pengetahuan Anda dan periksa jawaban yang dikomentari setelah umpan balik untuk menjawab pertanyaan Anda.
pertanyaan 1
(Mackenzie-SP)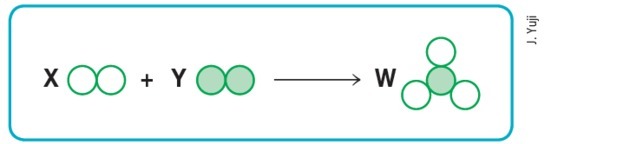
Dengan asumsi bahwa lingkaran kosong dan lingkaran berisi masing-masing berarti atom yang berbeda, maka skemanya di atas akan mewakili reaksi kimia yang seimbang jika kita mengganti huruf X, Y, dan W, masing-masing, dengan nilai:
a.1, 2 dan 3.
b) 1, 2 dan 2.
c.2, 1 dan 3.
d.3, 1 dan 2.
e.3, 2 dan 2.
Alternatif d) 3, 1 dan 2.
langkah pertama: Kami menetapkan huruf untuk membuat persamaan lebih mudah dipahami.
langkah ke-2: kami menambahkan indeks untuk mengetahui siapa yang memiliki atom terbanyak dalam persamaan.
| ITU | |
| B |
A dan B hanya muncul sekali di setiap anggota persamaan. Namun, jika kita menambahkan indeks, kita melihat bahwa A memiliki nilai tertinggi. Karena itu, kami memulai penyeimbangan untuknya.
langkah ke-3: Kami menyeimbangkan elemen A dengan mengubah indeks dan mengubahnya menjadi koefisien.
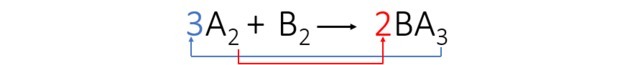
Kami mengamati bahwa elemen B secara otomatis seimbang dan koefisien persamaan adalah: 3, 1 dan 2.
pertanyaan 2
(Unicamp-SP) Baca kalimat berikut dan ubah menjadi persamaan kimia (setara), menggunakan simbol dan rumus: “molekul gas nitrogen, mengandung dua atom nitrogen per molekul, bereaksi dengan tiga molekul diatomik, gas hidrogen, menghasilkan dua molekul gas amonia, yang terdiri dari tiga atom hidrogen dan satu dari nitrogen".
Balasan:
Mewakili atom yang dijelaskan dalam pertanyaan, kita dapat memahami bahwa reaksi terjadi sebagai berikut:
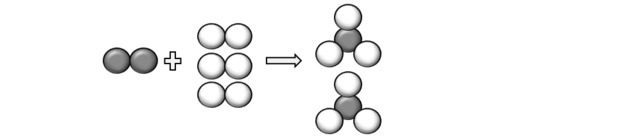
Jadi kita sampai pada persamaan:
pertanyaan 3
Hidrogen peroksida adalah senyawa kimia yang dapat terurai, membentuk air dan oksigen, sesuai dengan persamaan kimia di bawah ini.
Mengenai reaksi ini, persamaan yang disetarakan dengan benar adalah:
ah2HAI2 → The2 + H2HAI
b) 2 jam2HAI2 → The2 + 2H2HAI
c) H2HAI2 → 2O2 + H2HAI
d) 2 jam2HAI2 → 2O2 + 2H2HAI
Alternatif yang benar: b) 2H2HAI2 → The2 + 2H2HAI
Perhatikan bahwa hidrogen peroksida adalah bahan kimia yang terdiri dari atom dari dua unsur kimia: hidrogen dan oksigen.
Setelah reaksi dekomposisi, Anda harus memiliki jumlah atom yang sama dari dua unsur dalam reaktan dan produk. Untuk ini, kita perlu menyeimbangkan persamaan.
Perhatikan bahwa kita memiliki 2 atom hidrogen dalam reaktan (H2HAI2) dan dua atom dalam hasil kali (H2HAI). Namun, oksigen memiliki dua atom dalam reaktan (H2HAI2) dan tiga atom dalam produk (H2O dan O2).
Jika kita menempatkan koefisien 2 sebelum hidrogen peroksida, kita menggandakan jumlah atom unsur.
Perhatikan bahwa jika kita memasukkan koefisien yang sama dengan rumus air, kita memiliki jumlah atom yang sama di kedua sisi.
Oleh karena itu, persamaan kimia yang seimbang dengan benar adalah 2H2HAI2 → The2 + 2H2HAI.
pertanyaan 4
(UFPE) Perhatikan reaksi kimia di bawah ini.
Kita dapat mengatakan bahwa:
a) semua seimbang.
b) 2, 3 dan 4 seimbang.
c) hanya 2 dan 4 yang seimbang.
d) hanya 1 yang tidak seimbang.
e) tidak ada yang seimbang dengan benar, karena keadaan fisik reaktan dan produk berbeda.
Alternatif b) 2, 3 dan 4 seimbang.
Alternatif 1 dan 5 salah karena:
- Persamaan 1 tidak seimbang, keseimbangan yang benar adalah:
- Persamaan 5 salah karena senyawa yang terbentuk dalam reaksi adalah H2HANYA3.
membentuk H2HANYA4 harus dimasukkan dalam persamaan oksidasi SO2.
pertanyaan 5
(Mackenzie-SP) Dipanaskan hingga 800 °C, kalsium karbonat terurai menjadi kalsium oksida (kapur perawan) dan karbon dioksida. Persamaan seimbang yang benar, yang sesuai dengan fenomena yang dijelaskan, adalah:
(Diberikan: Ca — logam alkali tanah.)
Alternatif c)
Kalsium merupakan logam alkali tanah dan untuk memiliki kestabilan kalsium membutuhkan 2 elektron (Ca2+), yang merupakan muatan oksigen (O2-).
Dengan demikian, atom kalsium berikatan dengan atom oksigen dan senyawa yang terbentuk adalah CaO, yang merupakan kapur tohor.
Produk lainnya adalah karbon dioksida (CO2). Keduanya dibentuk oleh kalsium karbonat (CaCO3).
Masukkan ke dalam persamaan:
Kami mencatat bahwa jumlah atom sudah benar dan tidak perlu diseimbangkan.
pertanyaan 6
(UFMG) Persamaan tidak seimbang. Menyeimbangkannya dengan bilangan sekecil mungkin, jumlah koefisien stoikiometrinya adalah:
a) 4
b) 7
c) 10
d) 11
e) 12
Alternatif e) 12
Dengan menggunakan metode percobaan, urutan penyeimbangan akan menjadi:
langkah pertama: Karena unsur yang hanya muncul sekali di setiap anggota dan memiliki indeks tertinggi adalah kalsium, kami mulai menyeimbangkannya.
langkah ke-2: Kami mengikuti penyeimbangan oleh PO radical radikal43-, yang juga hanya muncul sekali.
langkah ke-3: kita menyeimbangkan hidrogen.
Dengan ini, kami mengamati bahwa secara otomatis jumlah oksigen telah disesuaikan dan keseimbangan persamaannya adalah:
Mengingat bahwa ketika koefisien adalah 1 Anda tidak perlu menuliskannya dalam persamaan.
Menambahkan koefisien yang kita miliki:
pertanyaan 7
Pembakaran adalah jenis reaksi kimia di mana energi dilepaskan dalam bentuk panas.
Dalam pembakaran sempurna suatu zat yang dibentuk oleh karbon dan hidrogen, karbon dioksida dan air terbentuk.
Amati reaksi pembakaran hidrokarbon dan jawablah persamaan di bawah ini yang tidak seimbang:
a) CH4 + 2O2 → CO2 + 2H2HAI
b) C3H8 +502 → 3CO2 + 4H2HAI
c) C4H10 +13/3O2 → 4CO2 + 5 jam2HAI
d) C2H6 + 7/2O2 → 2CO2 + 3H2HAI
Jawaban salah: c) C4H10 +13/3O2 → 4CO2 + 5 jam2HAI
Untuk menyetarakan persamaan kimia, pertama-tama mari kita lihat unsur mana yang muncul hanya sekali dalam setiap anggota persamaan.
Perhatikan bahwa karbon dan hidrogen hanya membentuk satu reaktan dan satu produk dalam setiap persamaan yang disajikan.
Jadi mari kita mulai menyeimbangkan dengan hidrogen, karena memiliki jumlah atom yang lebih banyak.
Oleh karena itu, urutan penyeimbangannya adalah:
- Hidrogen
- Karbon
- Oksigen
Hidrogen
Karena produk memiliki 2 atom hidrogen, kami memasukkan angka sebagai koefisien yang dikalikan dengan 2 menghasilkan jumlah atom hidrogen dalam reaktan.
a) CH4 + O2 → CO2 + 2H2HAI
b) C3H8 + O2 → CO2 + 4H2HAI
c) C4H10 + O2 → CO2 + 5H2HAI
d) C2H6 + O2 → CO2 + 3H2HAI
Karbon
Penyeimbangan dilakukan dengan mengubah indeks karbon dalam reaktan dan menggunakannya sebagai koefisien pada produk yang memiliki atom dari unsur ini.
a) CH4 + O2 → 1BERSAMA2 + 2H2HAI
b) C3H8 + O2 → 3BERSAMA2 + 4H2HAI
c) C4H10 + O2 → 4BERSAMA2 + 5 jam2HAI
d) C2H6 + O2 → 2BERSAMA2 + 3H2HAI
Oksigen
Menambahkan jumlah atom oksigen dalam produk yang terbentuk, kita menemukan jumlah atom unsur yang harus bereaksi.
Untuk itu, kita harus menempatkan sebagai koefisien angka yang dikalikan dengan 2 menghasilkan jumlah atom oksigen dalam produk.
a) CH4 + O2 → 1CO2 + 2H2HAI
2x = 2 + 2
2x = 4
x = 2
Jadi persamaan yang benar adalah: CH4 + 2HAI2 → 1CO2 + 2H2HAI.
b) C3H8 + O2 → 3CO2 + 4H2HAI
2x = 6 + 4
2x = 10
x = 5
Jadi persamaan yang benar adalah: C3H8 + 5HAI2 → 3CO2 + 4H2HAI
c) C4H10 + O2 → 4CO2 + 5 jam2HAI
2x = 8 + 5
2x = 13
x = 13/2
Jadi persamaan yang benar adalah: C4H10 + 13/2HAI2 → 4CO2+ 5 jam2HAI
d) C2H6 + O2 → 2CO2 + 3H2HAI
2x = 4 + 3
2x = 7
x = 7/2
Jadi persamaan yang benar adalah: C2H6 + 7/2HAI2 → 2CO2 + 3H2HAI
Persamaan yang benar seimbang adalah:
a) CH4 + 2O2 → CO2 + 2H2HAI
b) C3H8 +502 → 3CO2 + 4H2HAI
c) C4H10 + 13/2O2 → 4CO2 + 5 jam2HAI
d) C2H6 + 7/2O2 → 2CO2 + 3H2HAI
Jadi, alternatif c) C4H10 +13/3O2 → 4CO2 + 5 jam2Masalahnya, itu tidak memiliki keseimbangan yang benar.
pertanyaan 8
(Enem 2015) Batu kapur adalah bahan yang tersusun dari kalsium karbonat, yang dapat bertindak sebagai penyerap sulfur dioksida (SO2), polutan udara yang penting. Reaksi yang terlibat dalam proses tersebut adalah aktivasi batugamping, melalui kalsinasi, dan fiksasi SO .2 dengan pembentukan garam kalsium, seperti yang diilustrasikan oleh persamaan kimia yang disederhanakan.
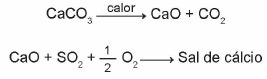
Mengingat reaksi yang terlibat dalam proses desulfurisasi ini, rumus kimia garam kalsium sesuai dengan:
Alternatif b)
Sebagai reaksi seimbang, atom dalam reaktan harus dalam jumlah yang sama dalam produk. Jadi,
Garam yang terbentuk terdiri dari:
1 atom kalsium = Ca
1 atom belerang = S
4 atom oksigen = O4
Oleh karena itu, rumus kimia garam kalsium sesuai dengan CaSO4.
pertanyaan 9
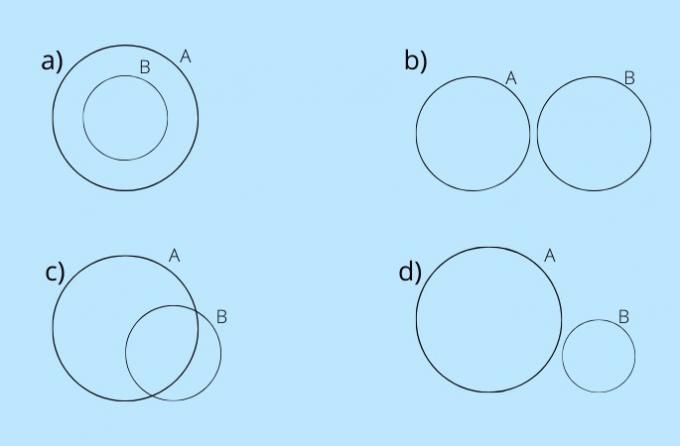
(UFPI) Reaksi X dengan Y ditunjukkan di bawah ini. Tentukan persamaan mana yang paling mewakili persamaan kimia yang seimbang.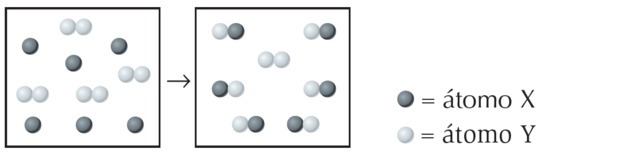
Alternatif a)
Pada gambar, kita mengamati bahwa spesies X adalah atom tunggal sedangkan Y adalah diatomik, yaitu, dibentuk oleh penggabungan 2 atom. Jadi X bereaksi dengan Y2.
Produk yang terbentuk diwakili oleh XY, persamaan menjadi tidak seimbang:
Kami menyeimbangkan persamaan sebagai berikut:
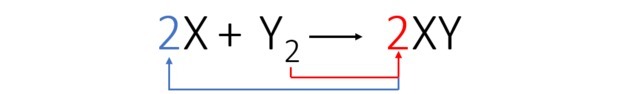
Menurut persamaan yang seimbang, gambar di bawah ini menunjukkan kepada kita bagaimana reaksi terjadi dan proporsinya.
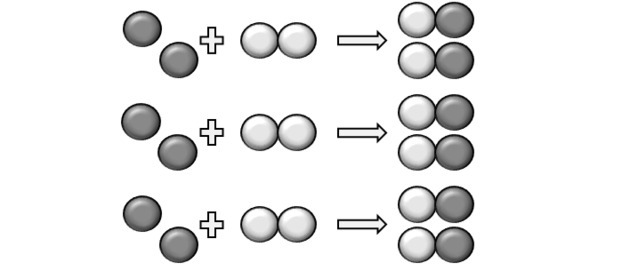
Agar reaksi terjadi harus ada rasio tetap dan oleh karena itu beberapa senyawa mungkin tidak bereaksi. Inilah yang ditunjukkan oleh gambar, karena dalam produk kita melihat bahwa Y2 tidak bereaksi.
pertanyaan 10
(Enem 2010) Mobilisasi untuk mempromosikan planet yang lebih baik bagi generasi mendatang semakin sering dilakukan. Sebagian besar alat transportasi massal saat ini didukung oleh pembakaran bahan bakar fosil. Sebagai contoh beban yang ditimbulkan oleh praktik ini, cukup diketahui bahwa sebuah mobil menghasilkan rata-rata sekitar 200 gram karbon dioksida per km yang ditempuh.
Majalah Pemanasan Global. Tahun 2, 8. Publikasi Instituto Brasileiro de Cultura Ltda.
Salah satu penyusun utama bensin adalah oktan (C8H18). Melalui pembakaran energi oktan dimungkinkan, memungkinkan mobil untuk mulai bergerak. Persamaan yang mewakili reaksi kimia dari proses ini menunjukkan bahwa:
a) oksigen dilepaskan dalam proses, dalam bentuk O2.
b) koefisien stoikiometri untuk air adalah 8 sampai 1 oktan.
c) dalam proses ada konsumsi air, sehingga energi dilepaskan.
d) koefisien stoikiometri untuk oksigen adalah 12,5 hingga 1 oktan.
e) koefisien stoikiometri untuk karbon dioksida adalah 9 hingga 1 oktan
Alternatif d) koefisien stoikiometri untuk oksigen adalah 12,5 hingga 1 oktan.
Saat menyeimbangkan persamaan, kami menemukan koefisien berikut:
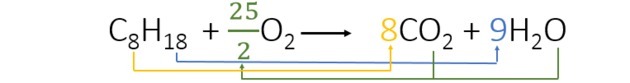
- Kami memulai penyeimbangan dengan hidrogen yang hanya muncul sekali di setiap anggota dan memiliki indeks yang lebih tinggi. Karena ada 18 atom hidrogen yang bereaksi, ada 2 dalam produk, jadi kita perlu menambahkan angka yang dikalikan dengan 2 menghasilkan 18. Jadi 9 adalah koefisiennya.
- Kemudian kita tambahkan koefisien 8 di depan CO2 memiliki 8 karbon di setiap anggota persamaan.
- Akhirnya, tambahkan saja jumlah oksigen dalam produk dan temukan nilai yang dikalikan dengan 2 menghasilkan 25 atom oksigen. Jadi kami memilih 25/2 atau 12,5.
Jadi, untuk pembakaran 1 oktan 12,5 oksigen dikonsumsi.
pertanyaan 11
(Fatec-SP) Karakteristik penting dari pupuk adalah kelarutannya dalam air. Oleh karena itu, industri pupuk mengubah kalsium fosfat, yang kelarutannya dalam air sangat rendah, menjadi senyawa yang jauh lebih mudah larut, yaitu kalsium superfosfat. Proses ini diwakili oleh persamaan:
dimana nilai x, y, dan z berturut-turut adalah:
a.4, 2 dan 2.
b.3, 6 dan 3.
c.2, 2 dan 2.
d) 5, 2 dan 3.
e.3, 2 dan 2.
Alternatif e) 3, 2 dan 2.
Menggunakan metode aljabar, kami membentuk persamaan untuk setiap elemen dan menyamakan jumlah atom dalam reaktan dengan jumlah atom dalam produk. Karena itu:
Persamaan seimbang:
pertanyaan 12
Setarakan persamaan di bawah ini dengan menggunakan metode percobaan.
Balasan:
Persamaan ini terdiri dari unsur hidrogen dan klorin. Kami menyeimbangkan elemen hanya dengan menambahkan koefisien 2 di depan produk.
Persamaan tidak perlu disetarakan, karena jumlah atom sudah disesuaikan.
Fosfor memiliki dua atom dalam reaktan, jadi untuk menyeimbangkan elemen ini kita menyesuaikan jumlah asam fosfat dalam produk menjadi 2H3DEBU4.
Setelah itu, kami mengamati bahwa hidrogen memiliki 6 atom dalam produk, kami menyeimbangkan jumlah elemen ini dengan menambahkan koefisien 3 ke reaktan yang mengandungnya.
Dengan langkah-langkah sebelumnya, jumlah oksigen ditetapkan.
Melihat persamaan kita melihat bahwa jumlah hidrogen dan bromin dalam produk adalah dua kali lipat jika ada dalam reagen, jadi kami menambahkan koefisien 2 ke HBr untuk menyeimbangkan keduanya elemen.
Klorin memiliki 3 atom dalam produk dan hanya 1 dalam reaktan, jadi kami menyeimbangkan menempatkan koefisien 3 sebelum HCl.
Hidrogen memiliki 3 atom dalam reaktan dan 2 atom dalam produk. Untuk menyesuaikan jumlah, kami mengubah indeks H2 dalam koefisien, kita kalikan dengan 3 yang sudah ada di HCl dan kita mendapatkan hasil 6HCl.
Kami menyesuaikan jumlah klorin dalam produk untuk juga memiliki 6 atom dan mendapatkan 2AlCl3.
Aluminium memiliki 2 atom dalam produk, kami menyesuaikan jumlah dalam reaktan menjadi 2Al.
Kami menyeimbangkan jumlah hidrogen dalam produk menjadi 3H2 dan kami menyesuaikan jumlah 6 atom unsur itu di setiap suku persamaan.
Dalam persamaan radikal nitrat (NO3-) memiliki indeks 2 dalam produk, kami mengubah indeks menjadi koefisien dalam reaktan untuk 2AgNO3.
Jumlah perak perlu disesuaikan, karena sekarang memiliki 2 atom dalam reagen, jadi kita memiliki 2Ag dalam produk.
Dalam reaktan kita memiliki 4 atom hidrogen dan untuk menyeimbangkan unsur ini kita menambahkan koefisien 2 pada produk HCl.
Klorin sekarang memiliki 4 atom dalam produk, jadi kami menyesuaikan jumlah dalam reagen menjadi 2Cl2.
Kami memiliki 6 atom hidrogen dalam reaktan dan untuk menyeimbangkan elemen ini kami menyesuaikan jumlah air menjadi 3H2HAI.
Kami memiliki 2 atom karbon dalam reaktan dan untuk menyeimbangkan elemen ini kami menyesuaikan jumlah karbon dioksida menjadi 2CO2.
Oksigen perlu memiliki 7 atom dalam reaktan dan untuk menyeimbangkan elemen ini kita menyesuaikan jumlah molekul oksigen menjadi 3O2.
Melihat persamaan, radikal nitrat (NO3-) memiliki indeks 2 dalam produk. Kami mengubah indeks menjadi koefisien 2 dalam reagen AgNO3.
Kami memiliki 2 atom perak dalam reaktan dan untuk menyeimbangkan elemen ini kami menyesuaikan jumlah perak klorida dalam produk menjadi 2AgCl.
Kami memiliki 3 atom kalsium dalam produk dan untuk menyeimbangkan elemen ini kami menyesuaikan jumlah kalsium nitrat dalam reagen menjadi 3Ca (NO3)2.
Kami kemudian ditinggalkan dengan 6 radikal NO3- dalam reaktan dan untuk menyeimbangkan radikal ini kita menyesuaikan jumlah asam nitrat dalam produk menjadi 6HNO3.
Kami sekarang memiliki 6 atom hidrogen dalam produk dan untuk menyeimbangkan elemen ini kami menyesuaikan jumlah asam fosfat dalam reagen menjadi 2H3DEBU4.
Pelajari lebih lanjut tentang perhitungan dengan persamaan kimia di:
- Menyeimbangkan persamaan kimia
- Stoikiometri
- Perhitungan stoikiometri
- Latihan Stoikiometri
- Latihan tabel periodik