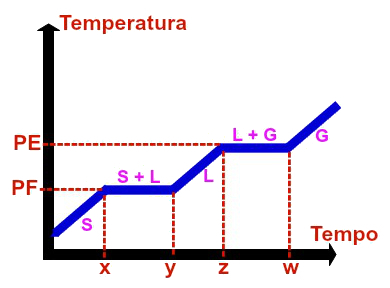
Titik leleh dan titik didih menunjukkan suhu di mana suatu zat berubah keadaan pada tekanan tertentu.
Dalam kasus titik leleh, zat berubah dari keadaan padat ke keadaan cair. Titik didih mengacu pada perubahan dari keadaan cair ke keadaan gas.
Misalnya, es mulai berubah menjadi air dalam bentuk cair ketika suhunya sama dengan 0°C. Oleh karena itu, titik leleh air adalah 0 °C (di bawah tekanan 1 atmosfer).
Untuk berubah dari cair menjadi uap, air harus mencapai suhu 100 °C. Jadi, titik didih air adalah 100 °C (di bawah tekanan 1 atmosfer).

Titik fusi
Ketika suatu zat dalam keadaan padat menerima panas, ada peningkatan derajat agitasi molekulnya. Akibatnya suhunya juga meningkat.
Setelah mencapai suhu tertentu (titik lebur), agitasi molekul sedemikian rupa sehingga memutuskan ikatan internal antara atom dan molekul.
Pada titik ini, zat tersebut mulai berubah wujudnya dan akan berubah wujud menjadi cair jika terus menerima kalor.
Selama Fusi suhunya tetap konstan, karena panas yang diterima digunakan semata-mata untuk perubahan keadaan.

Kalor per satuan massa yang diperlukan untuk mengubah fasa disebut panas laten fusi (Lf) dan merupakan karakteristik zat.
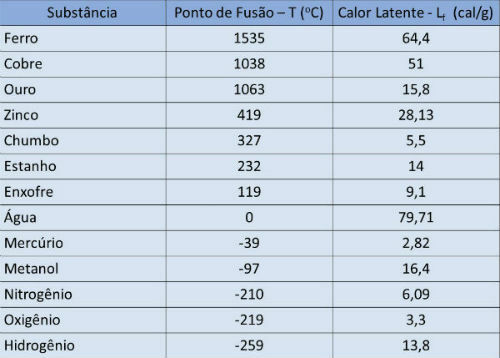
Titik lebur dan tabel panas laten
Pada tabel di bawah ini kami menunjukkan suhu titik leleh dan panas laten beberapa zat untuk tekanan atmosfir.
Titik didih
ITU mendidih itu ditandai dengan perjalanan cepat dari cairan ke keadaan gas, dengan pembentukan uap (gelembung) di dalam cairan.
Seperti dalam fusi, ada suhu (titik didih) di mana zat tertentu berubah dari cair menjadi gas.
Agar ini terjadi, zat harus menerima panas. Selama seluruh perubahan fase, suhu tetap konstan.
panas laten penguapan (Lv) adalah jumlah kalor per satuan massa yang diperlukan suatu zat untuk berubah fasa.
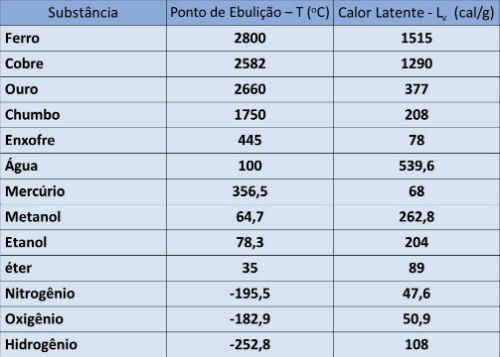
Titik didih dan tabel panas laten
Pada tabel di bawah, kami menunjukkan suhu titik didih dan panas laten penguapan beberapa zat pada tekanan atmosfer.
Gangguan tekanan
Suhu titik leleh dan titik didih tergantung pada tekanan yang diberikan pada zat.
Secara umum, zat bertambah volumenya ketika mereka mengalami fusi. Fakta ini berarti bahwa semakin tinggi tekanan, semakin tinggi suhu zat untuk mengubah fasenya.
Pengecualian terjadi pada beberapa zat, termasuk air, yang volumenya berkurang saat meleleh. Dalam hal ini, tekanan yang lebih tinggi akan menurunkan titik leleh.

Penurunan tekanan menyebabkan titik didih suatu zat menjadi lebih rendah, artinya zat tersebut akan mendidih pada suhu yang lebih rendah.
Misalnya, di tempat-tempat di atas permukaan laut, air mendidih pada suhu di bawah 100 °C. Akibatnya, dibutuhkan waktu lebih lama untuk memasak di tempat-tempat ini daripada di tempat-tempat di permukaan laut.
Baca juga:
- Perubahan Keadaan Fisik
- Timbangan Termometrik
- Timbangan Termometrik - Latihan
- Keadaan Fisik Air
- Diagram fase
- Pemadatan
- Kondensasi
- Sifat koligatif
- Sifat Periodik
- Penguapan
- Latihan pada Tabel Periodik