HAI sinar atom unsur adalah sifat periodik yang menentukan jari-jari atom yang bervariasi tergantung pada posisi unsur dalam tabel periodik.
Dengan demikian, mereka dapat meningkat dan menurun seiring nomor atom (Z) unsur yang sesuai dengan jumlah proton yang ada dalam inti atom.
Singkatnya, jari-jari atom sesuai dengan setengah jarak antara inti dua atom tetangga, yang dinyatakan sebagai berikut:
r = d/2
dari mana:
r = radius
d = jarak antar nuklir
Umumnya, jari-jari atom diukur dalam pikometer (pm), sub-kelipatan meter (1 pikometer = 10-12 m.). Perhatikan bahwa ketika referensi bukan atom tetapi ion, jari-jari yang ditemukan adalah jari-jari ion.
Variasi Jari-jari Atom
Dalam tabel periodik, pertumbuhan jari-jari atom dapat dilihat pada gambar berikut:
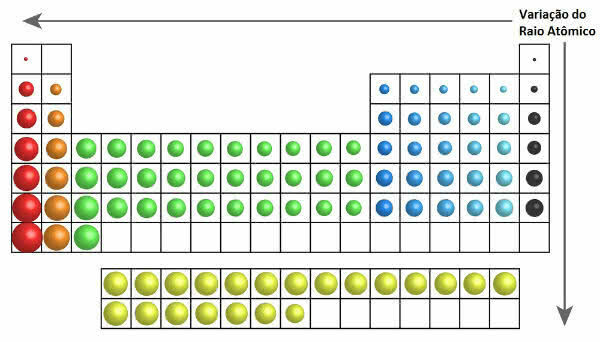 Variasi Jari-jari Atom dalam Tabel Periodik
Variasi Jari-jari Atom dalam Tabel Periodik
Jadi, secara vertikal (keluarga atau kelompok) jari-jari atom meningkat dari atas ke bawah. Pada horizontal (titik), mereka meningkat dari kanan ke kiri.
Lihat variasi terbalik di Afinitas Elektronik dan keelektronegatifan.
Energi ionisasi
ITU energi ionisasi (atau potensial) itu juga merupakan sifat periodik yang menentukan energi yang dibutuhkan untuk menggeser elektron, yang dinyatakan dalam elektron volt (eV).
Baca juga: Sifat Periodik.
Periksa pertanyaan ujian masuk dengan resolusi komentar di: Latihan pada Tabel Periodik.


