Hidrokarbon, juga disebut hidrogen karbida, adalah senyawa organik yang komposisinya hanya memiliki atom karbon (C) dan dari hidrogen (H), sehingga memiliki rumus umum CxHkamu.
Hidrokarbon terdiri dari struktur karbon tempat atom hidrogen berikatan Ikatan kovalen.
Ini adalah senyawa yang paling penting dalam kimia organik.
Semua jenis hidrokarbon mudah teroksidasi, sehingga melepaskan panas. Kebanyakan dari mereka tidak larut dalam air.
Hidrokarbon alami adalah senyawa kimia yang terbentuk di dalam Bumi (lebih dari 150 km dari kedalaman) pada tekanan tinggi dan mencapai zona tekanan rendah melalui proses geologi.
Di mana hidrokarbon ditemukan?
Sumber utama hidrokarbon adalah minyak bumi. Karena itu, hidrokarbon hadir dalam beberapa turunan seperti: minyak tanah, parafin, gas alam, Bensin, vaselin, minyak diesel, elpiji (Gas minyak cair), polimer (seperti plastik dan karet), antara lain.
Senyawa organik ini merupakan 48% dari matriks energi Brasil.
Rantai karbon yang merupakan bagian dari komposisi hidrokarbon adalah tetravalen, yaitu, dapat membuat empat koneksi.
Karbon dapat berikatan dengan atom karbon lain dan dengan hidrogen melalui tautan sederhana, ganda atau tiga kali lipat.
Klasifikasi hidrokarbon
Klasifikasi hidrokarbon didasarkan pada tiga kekhususan: a untuk m dari rantai karbon utama, Koneksi dari rantai karbon, adanya radikal alkil dalam rantai karbon dan adanya heteroatom membagi rantai karbon.
tahu lebih banyak tentang hidrogen.
Bentuk rantai karbon utama
Berkenaan dengan bentuk rantai karbon utama, klasifikasi hidrokarbon dibagi menjadi: alifatik dan berhubung dgn putaran.
Lihat apa yang terdiri dari masing-masing bentuk rantai karbon ini.
hidrokarbon alifatik
Hidrokarbon alifatik dibentuk oleh rantai karbon Buka atau asiklik. Dalam rantai ini, karbon adalah terminal.
Contoh:
alkana
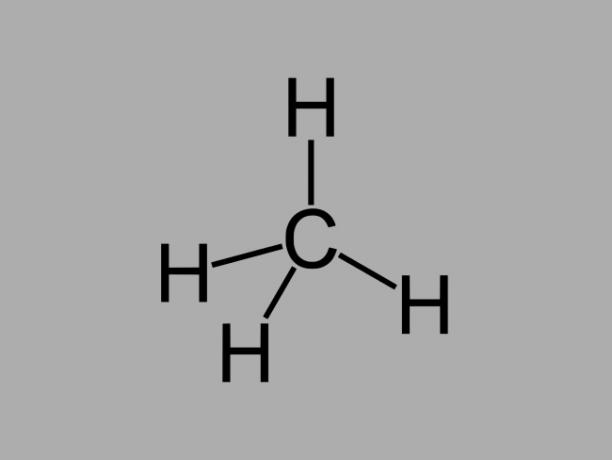
Hidrokarbon alkana, juga disebut parafin atau parafin, adalah senyawa berminyak di mana hanya ada ikatan tunggal antara karbon.
Rumus umum alkana adalah CtidakH2tidak + 2 (n = bilangan bulat apa saja).
alkena
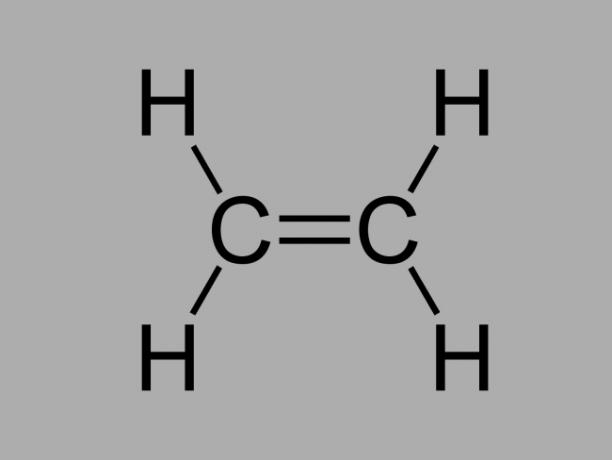
Disebut juga olefin, alkena atau etilen hidrokarbon, alkena adalah senyawa yang kurang reaktif di mana ada ikatan rangkap antara karbon.
Rumus umum alkena adalah CtidakH2tidak.
alkuna
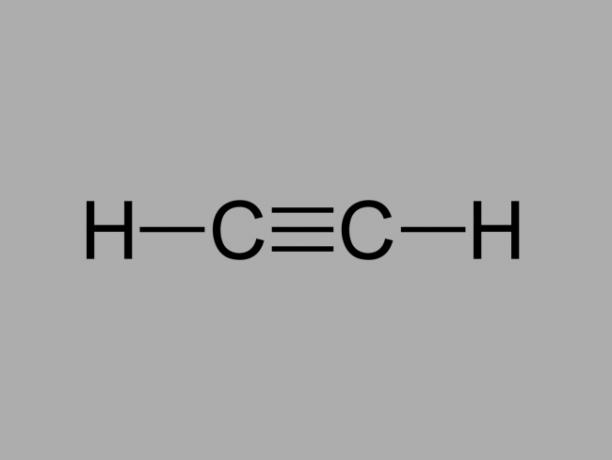
Disebut juga methylacetylene, alkuna adalah hidrokarbon di mana ikatan antara karbon adalah rangkap tiga.
Rumus umum alkuna adalah CtidakH2tidak-2.
alkalin

Juga disebut diena atau diolefin, alkadiena adalah hidrokarbon di mana ikatan antara karbon adalah ganda.
Rumus umum alkana adalah CtidakH2tidak-2.
Hidrokarbon siklik
Hidrokarbon siklik dibentuk oleh rantai karbon tertutup atau siklik. Rantai ini tidak memiliki karbon terminal.
Contoh:
siklon
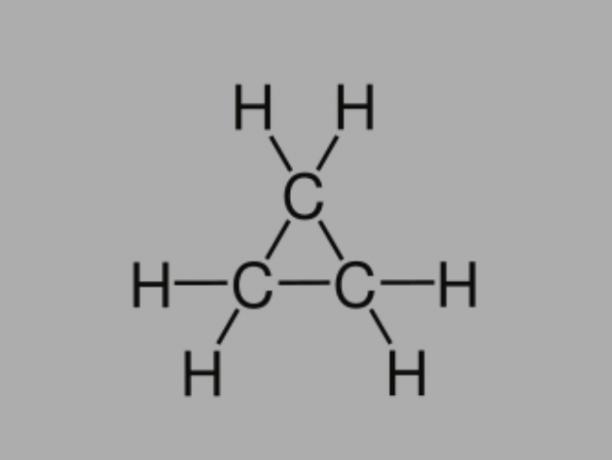
Disebut juga sikloalkana, sikloparafin atau hidrokarbon naftenat, cyclane adalah hidrokarbon jenuh, terdiri dari ikatan tunggal.
Ini memiliki rantai karbon tertutup dan rumus umumnya adalah CtidakH2tidak.
siklonik

Disebut juga sikloalkena, cyclenes adalah hidrokarbon tak jenuh, terdiri dari ikatan rangkap.
Sebuah cyclene memiliki rantai karbon tertutup dan rumus umumnya adalah CtidakH2tidak−2.
pengendara sepeda
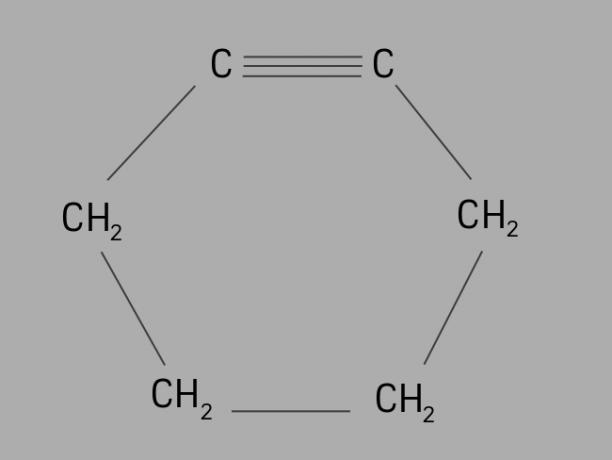
Disebut juga sikloalkuna atau sikloalkuna, siklin adalah hidrokarbon siklik dan tak jenuh.
Ini dibentuk oleh rantai karbon tertutup, dengan ikatan rangkap tiga dan rumus umumnya adalah CtidakH2tidak-4.
Aromatik

atau

Disebut juga arena, hidrokarbon aromatik adalah senyawa tak jenuh yang dibentuk oleh ikatan rangkap.
Aromatik memiliki rantai karbon tertutup atau siklik dan rumus umumnya adalah C6H6.
Jenis ikatan rantai karbon
Tergantung pada jenis hubungan rantai karbon, hidrokarbon dapat diklasifikasikan menjadi: jenuh atau tak jenuh.
Lihat di bawah ini terdiri dari apa masing-masing klasifikasi ini.
Hidrokarbon jenuh
Hidrokarbon jenuh dibentuk oleh tautan sederhana.
Contoh: alkana, siklan.
hidrokarbon tak jenuh
Hidrokarbon tak jenuh dibentuk oleh ikatan rangkap atau tiga kali lipat.
Contoh: alkena, alkuna, alkadiena.
Kehadiran radikal alkil
Mengenai keberadaan radikal alkil, hidrokarbon dapat memiliki rantai karbon normal atau bercabang.
rantai karbon biasa
Hidrokarbon rantai karbon normal tidak memiliki radikal alkil.
Contoh: pentana
rantai karbon bercabang
Ketika suatu hidrokarbon memiliki rantai karbon bercabang, itu berarti rantai karbon utamanya memiliki radikal alkil.
Contoh: metilpropana
Kehadiran heteroatom yang membagi rantai karbon
Rantai karbon berurutan mungkin atau mungkin tidak terpecah tergantung pada keberadaan heteroatom.
Rantai karbon homogen
Ketika suatu hidrokarbon memiliki rantai karbon utama yang homogen, itu berarti rantai ini tidak terbagi oleh heteroatom.
Rantai karbon heterogen
Jika suatu hidrokarbon memiliki rantai karbon utama yang heterogen, rantai ini memiliki perpecahan rantai karbon oleh heteroatom.
Tata nama hidrokarbon
Nomenklatur hidrokarbon didefinisikan melalui kombinasi tiga bagian:

Awalan menunjukkan jumlah karbon, perantara mengidentifikasi jenis ikatan, dan akhiran menunjukkan fungsi senyawa tersebut (dalam hal ini, kelas hidrokarbon).
Lihat di bawah untuk daftar awalan dan zat antara yang digabungkan untuk menunjuk hidrokarbon.
Daftar awalan
| Jumlah karbon | Awalan |
|---|---|
| 1 | bertemu- |
| 2 | dan- |
| 3 | Menopang- |
| 4 | Tapi- |
| 5 | terpendam- |
| 6 | Hex- |
| 7 | Hept- |
| 8 | Oktober- |
| 9 | Non- |
| 10 | Desember- |
Daftar perantara
| Jenis Koneksi | Perantara |
|---|---|
| Hanya satu panggilan | -sebuah- |
| Pasangan | -en- |
| tiga kali lipat | -di- |
| dua pasang | -dien- |
Lihatlah beberapa contoh penamaan hidrokarbon.
Contoh:
CH3 – CH2 – CH2 – CH3
Pada bentuk struktur di atas, kita dapat melihat senyawa berkarbon 4 yang hanya memiliki ikatan tunggal (ditunjukkan dengan simbol “–”).
- Awalan untuk 4 karbon = tapi-
- Perantara untuk pengikatan tunggal= -an-
- Akhiran dari hidrokarbon = -o
Lihat bahwa persatuan awalan + perantara + akhiran memunculkan nama BUTAN.
CH2 = CH2
Bentuk struktur di atas memiliki 2 karbon dan 1 ikatan rangkap (ditunjukkan dengan simbol “=”).
- Awalan untuk 2 karbon = et-
- Perantara untuk ikatan rangkap= -en-
- Akhiran dari hidrokarbon = -o
Lihat bahwa persatuan awalan + perantara + akhiran memunculkan nama ETENA.
CH2 = CH - CH2 – CH3
CH3 – CH = CH2 – CH3
Perhatikan bahwa kedua bentuk struktur di atas memiliki 4 karbon dan 1 ikatan rangkap (ditunjukkan dengan simbol “=”).
Dengan demikian, kami memiliki:
- Awalan untuk 4 karbon = tapi-
- Perantara untuk ikatan rangkap= -en-
- Akhiran dari hidrokarbon = -o
Lihat bahwa persatuan awalan + perantara + akhiran akan memunculkan nama BUTEN untuk dua bentuk struktural.
Namun, perhatikan bahwa bentuk strukturalnya tidak identik, sehingga nomenklaturnya tidak bisa keduanya.
Perbedaan antara kedua bentuk struktur tersebut terletak pada letak ikatan rangkapnya.
Dalam hal ini, kita harus memberi nomor pada karbon dalam rantai dari ujung yang paling dekat dengan rangkapnya. Oleh karena itu, dalam kasus yang bersangkutan, kita harus memberi nomor dari kiri ke kanan.
Di CH2 = CH - CH2 – CH3:
- CH2 akan menjadi 1
- CH akan menjadi 2
- CH2 akan menjadi 3
- CH3 akan menjadi 4
Perhatikan bahwa ikatan rangkap berada di antara karbon 1 ini adalah karbon 2.
Kita harus menggunakan angka terkecil (1) untuk menemukan ikatan rangkap: BUTEN -1
Di CH3 – CH = CH2 – CH3:
- CH3 akan menjadi 1
- CH akan menjadi 2
- CH2 akan menjadi 3
- CH3 akan menjadi 4
Perhatikan bahwa ikatan rangkap berada di antara karbon 2 ini adalah karbon 3.
Kita harus menggunakan bilangan terkecil (2) untuk menemukan ikatan rangkap: BUTENA -2
Berdasarkan IUPAC (Persatuan Internasional Kimia Murni dan Terapan – Persatuan Internasional Kimia Murni dan Terapan), lokasi harus ditunjukkan sedikit sebelum terletak (dalam kasus formal struktural di atas, ikatan rangkap, diwakili oleh perantara “-en-”).
Dengan itu, kita punya cara kedua, yang omong-omong paling benar, yaitu menulis nomenklatur bentuk-bentuk struktural yang ada.
CH2 = CH - CH2 – CH3: BUTENE -1 atau BUT-1-ENO (bentuk yang lebih benar)
CH3 – CH = CH2 – CH3: BUTENE -2 atau BUT-2-ENE (bentuk yang lebih benar)
Belajar lebih tentang IUPAC dan tata nama.


