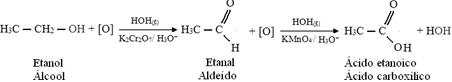
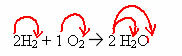Kapasitas yang dimiliki sambungan untuk menarik muatan listrik didefinisikan sebagai Polaritas, yang memiliki karakter berbeda tergantung pada sambungan di mana ia berada.
Mengenai ikatan ion dan kovalen, manakah yang bersifat polar atau nonpolar?
Senyawa ionik bermuatan listrik: kation dan anion, yang masing-masing disebut kutub positif dan negatif. Ini diwakili oleh tanda-tanda + dan -. Zat ionik bereaksi dengan senyawa lain karena adanya kutub-kutub tersebut yang membuat ikatan menjadi tidak stabil. Contoh: ikatan ionik atom Klorin dan Natrium menimbulkan senyawa natrium klorida (Na+Cl-), yang dikenal sebagai garam meja.
Singkatnya: Setiap ikatan ion adalah ikatan polar.
Senyawa kovalen sebagian besar diklasifikasikan sebagai non-polar.
Tapi ingat: itu tidak berarti bahwa setiap senyawa kovalen adalah non-polar. Kutub berasosiasi dengan keelektronegatifan, jika ikatan kovalen antara atom-atom dengan keelektronegatifan yang sama, ikatan akan bersifat non-polar, karena tidak ada pembentukan kutub.
Contoh: senyawa kovalen C3H8 (Propana) adalah non-polar, mari kita lihat alasannya:
H H H
│ │ │
H C C C H
│ │ │
H H H
Perhatikan bahwa ikatan terjadi antara unsur-unsur yang sama, sehingga mereka memiliki skala elektronegativitas yang sama.
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Oleh Liria Alves
Lulus kimia
Tim Sekolah Brasil
Lihat lebih banyak:
Jangan lupa tentang elektronegativitas
Ketahui unsur mana yang lebih elektronegatif
kimia umum - Kimia - Sekolah Brasil
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
SOUZA, Liria Alves de. "Polaritas ikatan ionik dan kovalen"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/polaridade-das-ligacoes-ionica-covalente.htm. Diakses pada 27 Juni 2021.