Kita akan melihat dalam teks ini bagaimana a bagan dari perubahan keadaan fisik untuk setiap zat murni, bagaimana menafsirkan diagram jenis ini dan bagaimana grafik campuran direpresentasikan.
Untuk melakukan ini, mari kita perhatikan contoh air. Bayangkan kita mengambil segelas es pada suhu -10 C dan memulai proses pemanasan, di bawah tekanan 1 atm. Ketika suhu meningkat, dari -10 C ke -9 C, ke -8 C dan seterusnya, es akan tetap dalam keadaan padat hingga mencapai suhu 0 C.
Pada saat itu, ia mulai bergerak ke keadaan cair, yaitu, fusi mulai terjadi. Suhu tidak akan terus naik seperti sebelumnya, tetapi akan tetap konstan pada 0 °C sampai semua es mencair:

Setelah melebur semua padatan, suhu sistem akan terus meningkat hingga mencapai suhu 100°C. Pada suhu ini, air yang tadinya dalam keadaan cair akan mulai berubah menjadi uap, yaitu akan mendidih.
Seperti yang terjadi di titik fusi, pada titik didih, suhu juga akan tetap konstan sampai semua cairan berubah menjadi uap. Setelah itu, jika kita terus memanaskan sistem, suhu akan terus naik:
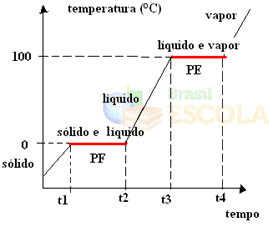
Siap! Ini adalah grafik atau diagram yang mewakili perubahan keadaan fisik air atau kurva pemanasannya. Jika itu adalah proses terbalik, kita akan memiliki kurva pendinginan air berikut:
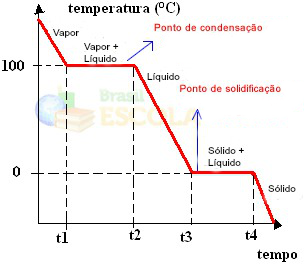
Aspek yang sangat penting dari grafik ini adalah bahwa mereka dibentuk oleh dua tingkat, yaitu, ada dua titik di mana suhu tetap konstan untuk sementara waktu. Ini selalu terjadi dalam perubahan keadaan zat murni. Satu-satunya perbedaan adalah nilai titik leleh dan titik didih.
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
Oksigen, misalnya, tidak seperti air, bukanlah cairan, tetapi gas pada suhu kamar (sekitar 20ºC). Ini karena titik lelehnya di permukaan laut adalah -223.0 °C dan titik didihnya -183.0 °C. Lihat bagan perubahan keadaan fisik Anda:

Grafis campuran umum
Jika kita memanaskan atau mendinginkan suatu campuran, titik leleh dan titik didihnya tidak akan sama ditentukan dan nilai konstan, yaitu, dua level yang diamati dalam grafik tidak akan terbentuk atas.
Perubahan keadaan fisik akan terjadi pada rentang suhu daripada jumlah yang tetap. Titik leleh, misalnya, akan dimulai pada suhu tertentu dan berakhir pada suhu lain, dan hal yang sama akan terjadi pada titik didih, seperti yang ditunjukkan pada grafik berikut:
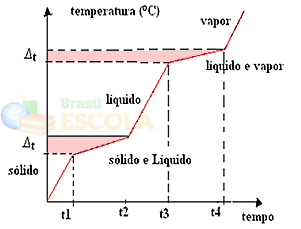
Dua pengecualian adalah campuran eutektik dan azeotropik. Lihat apa yang terjadi pada mereka:
a) Campuran eutektik
Campuran eutektik berperilaku seolah-olah itu adalah zat murni selama fusi, yaitu, pada saat itu, suhu tetap konstan dari awal hingga akhir perubahan keadaan agregasi.

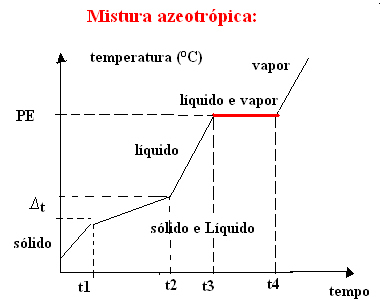
b.campuran azeotropik
Campuran azeotropik berperilaku seperti zat murni selama mendidih, yaitu, pada titik ini, suhu tetap konstan dari awal hingga akhir perubahan keadaan agregasi.
Oleh Jennifer Fogaa
Lulus kimia
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
FOGAÇA, Jennifer Rocha Vargas. "Grafik Perubahan Keadaan Fisik"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm. Diakses pada 28 Juni 2021.