Nomor atom, dilambangkan dengan huruf Z, sesuai dengan jumlah proton yang ada dalam inti atom suatu unsur kimia tertentu. Misalnya, nomor atom hidrogen adalah 1, yang berarti hanya memiliki 1 proton dalam inti atomnya.
Nomor atom biasanya muncul di sebelah simbol subskrip unsur kimia (di sudut kiri bawah). Contoh: 1H
Dalam keadaan dasar, nomor atom sama dengan jumlah elektron, karena dalam keadaan ini unsurnya adalah netral, oleh karena itu, jumlah muatan positif (proton) harus sama dengan jumlah muatan negatif (elektron) dari atom.
Nomor atom penting karena dialah yang menentukan karakteristik utama dan sifat-sifat elemen, serta perilaku dan lokasinya dalam Tabel Periodik. Unsur-unsur tercantum dalam Tabel Periodik dalam urutan nomor atom, yang biasanya muncul di atas unsur, seperti yang ditunjukkan di bawah ini. Perhatikan bahwa unsur pertama adalah hidrogen, H (Z = 1), diikuti oleh helium, He (Z = 2), kemudian datang litium, Li (Z = 3), dan seterusnya.
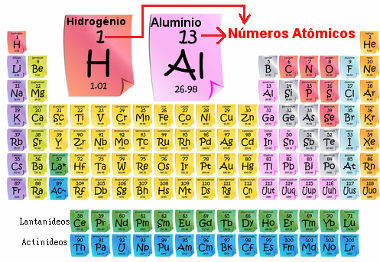
Nomor atom unsur dalam Tabel Periodik
Kita bahkan dapat mengkonseptualisasikan unsur kimia sebagai makhluk “kumpulan atom yang memiliki nomor atom sama”. Jadi, ketika kita berbicara, misalnya, tentang unsur kimia oksigen, kita berbicara tentang atom dengan nomor atom 8. Di bawah ini kita memiliki atom-atom unsur kimia dari periode 1 dan 2 dari Tabel Periodik dalam urutan nomor atom:

Unsur-unsur kimia dari periode 1 dan 2 dari Tabel Periodik dalam urutan nomor atom
Nomor atom awalnya ditentukan oleh fisikawan Inggris Henry Gwyn Jeffreys Moseley (1887-1915), dan ketika melakukan eksperimen yang melibatkan pemboman berbagai elemen ahli kimia dengan sinar-X, ia mengamati bahwa akar kuadrat dari frekuensi sinar-X yang dihasilkan oleh emisi inti atom berbanding lurus dengan nomor atom unsur dalam Tabel. Berkala. Dengan ini, ia menyimpulkan bahwa nomor atom terkait dengan sifat-sifat atom karena mewakili jumlah muatan positif dalam inti setiap atom.
Ikatan kimia tidak mempengaruhi nomor atom atom, karena hanya melibatkan elektron yang berada di elektrosfer. Namun, reaksi nuklir melibatkan inti atom dan karenanya nomor atom juga disertakan.
Misalnya, ketika partikel (terutama neutron sedang) dibombardir ke inti atom yang berat dan tidak stabil, inti itu adalah pecah dan menghasilkan dua inti atom yang lebih kecil, yaitu dengan jumlah proton dan neutron yang lebih kecil, melepaskan sejumlah besar energi.
Fusi nuklir, di sisi lain, adalah proses yang berlawanan, yaitu ketika dua inti kecil dan ringan bersatu, menghasilkan inti yang lebih besar dan lebih stabil, melepaskan jumlah energi yang lebih besar.
Jadi, setiap kali reaksi nuklir ini terjadi, unsur-unsur kimia baru berasal, karena nomor atom unsur awal berbeda dari nomor atom unsur akhir. Sebagai contoh, lihat di bawah bahwa fisi uranium-235 dengan nomor atom 92 menghasilkan barium (Z = 56), kripton (Z = 36) dan tiga neutron:

Reaksi fisi nuklir uranium-235
Oleh Jennifer Fogaa
Lulus kimia
Sumber: Sekolah Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-numero-atomico.htm


