Radioaktivitas adalah sifat yang dimiliki beberapa atom, seperti uranium dan radio, harus mengeluarkan secara spontan energi dalam bentuk partikel dan gelombang, menjadi unsur kimia lebih stabil dan ringan.
Jenis
Radioaktivitas muncul dengan sendirinya dua arah radiasi yang berbeda: partikel — alfa (α) dan beta (β); dan gelombang elektromagnetik — sinar gamma (γ).
sinar alfa: mereka adalah partikel positif yang terdiri dari dua proton dan dua neutron dan dengan daya penetrasi rendah.
sinar beta: adalah partikel negatif yang tidak mengandung massa yang terdiri dari elektron (massa diabaikan), dan daya penetrasinya lebih besar dari sinar alfa, tetapi lebih kecil dari sinar gamma.
Gamma: mereka adalah gelombang elektromagnetik energi tinggi dan, karena mereka bukan partikel, mereka juga tidak memiliki massa.
Baca juga: Rumus radioaktivitas
Jangan berhenti sekarang... Ada lagi setelah iklan ;)
hukum
Emisi radioaktif partikel mengikuti perilaku tertentu yang dijelaskan oleh hukum radioaktivitas (satu untuk partikel alfa dan satu untuk partikel beta), yang dijelaskan oleh ahli kimia Inggris
Frederick Soddydan oleh ahli kimia dan fisikawan Polandia Kazimierz Fajans.Hukum pertama radioaktivitas
Menurut hukum ini, ketika sebuah atom radioaktif memancarkan radiasi tipe alfa, itu akan menimbulkan atom baru dengan inti yang mengandung dua proton dan dua neutron kurang, total massa empat unit lebih kecil. Kami dapat mewakili hukum pertama radioaktivitas dengan persamaan umum berikut:
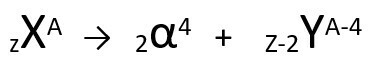
Persamaan umum dari hukum pertama radioaktivitas.
Mari kita lihat sebuah contoh:
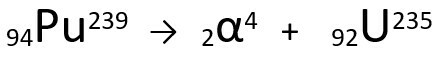
Persamaan yang mewakili emisi partikel oleh Plutonium-239.
Perhatikan bahwa, ketika memancarkan radiasi alfa, atom yang baru terbentuk, Uranium-235, memiliki nomor massa empat satuan lebih kecil dan nomor atom dua unit lebih kecil — persis nilai-nilai yang sesuai dengan partikel yang dipancarkan oleh inti plutonium. Untuk mempelajari lebih lanjut, kunjungi: Hukum Pertama Radioaktivitas atau Hukum Soddy Pertama.
Hukum radioaktivitas kedua
Hukum kedua berbicara tentang masalah beta. Ketika sebuah atom memancarkan partikel beta, yang terdiri dari elektron dan massa yang dapat diabaikan, massa atom sisa tidak berubah itu milikmu nomor atom bertambah satu satuan. Secara umum, kami mewakili sebagai berikut:
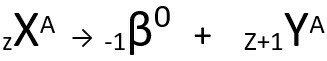
Persamaan umum dari hukum kedua radioaktivitas.
Lihat contohnya:
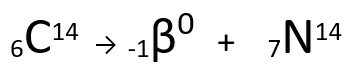
Persamaan yang mewakili emisi partikel β oleh Karbon-14.
Dapat dilihat bahwa atom nitrogen yang terbentuk memiliki massa yang sama dengan atom C-14, yaitu isobar, dan nomor atomnya bertambah satu satuan. peningkatan nomor atomdijelaskan oleh ilmuwan Henrico Fermi, yang mengusulkan bahwa salah satu dari neutron inti mengalami transmutasi, menurut persamaan berikut, menghasilkan Sebuahelektron(partikel beta yang dipancarkan), Sebuah neutrino(partikel subatomik tanpa muatan listrik dan tanpa massa, ) dan Sebuah proton(P).
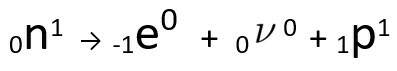
Persamaan yang mewakili transmutasi neutron, menurut hipotesis Fermi.
HAI elektron ini adalah neutrino dikeluarkan untuk keluar dari inti, tersisa hanya proton, yang menjelaskan kenaikan nomor atom Untuk mempelajarinya lebih lanjut, kunjungi: Hukum Kedua Radioaktivitas atau Hukum Kedua Soddy.
Baca juga: Perbedaan antara kontaminasi radioaktif dan iradiasi
aplikasi
meskipun pandangan negatif deposit pada radioaktivitas, ia memiliki aplikasi penting dalam kehidupan kita sehari-hari, misalnya dalam produksi dari listrikdi pembangkit listrik tenaga nuklir melalui pembelahandari atom radioaktif.
Saat ini, Brasil tidak menggunakan energi nuklir sebagai sumber energi utamanya, tetapi memiliki pembangkit nuklir (Angra 1 dan 2) yang berfungsi untuk memasok listrik ke negara tersebut. Kami juga dapat menyebutkan kencan materi ditemukan oleh para arkeolog menggunakan karbon-14.

Pembangkit Listrik Tenaga Nuklir Rio de Janeiro, Brasil
Peran mendasar lain yang dimainkan radioaktivitas terkait dengan bidang kedokteran, seperti dalam sinar Xdan di CT scan, dan juga dalam beberapa jenis pengobatan kanker.
Baca juga: Risiko utama pembangkit listrik tenaga nuklir bagi lingkungan
radioaktivitas alam
setiap hari kita terkena Itu jumlah kecil radiasi, baik buatan maupun alami. Radioaktivitas alam terjadi secara spontan di alam. Bagian dari radiasi yang kita terima ini berasal dari makanan yang dikonsumsi sehari-hari, seperti Radon-226 dan Potassium-40, yang disajikan dalam tingkat yang sangat rendah dan mereka tidak membahayakan kesehatan kita atau membahayakan nilai gizi makanan.
Proses memaparkan makanan pada emisi radioaktif ini dimaksudkan untuk: melestarikan makanan dan promosikan pertumbuhan tanaman. Beberapa contoh makanan yang memancarkan radiasi adalah: Kacang brazil, pisang, kacang-kacangan, daging merah, antara lain.
Penemuan
Studi tentang radioaktivitas dimulai dengan penelitian oleh fisikawan Jerman Wilhelm Röentgen, pada tahun 1895, ketika ia sedang menyelidiki efek daripendaran. Ilmuwan penting lainnya untuk pengembangan radioaktivitas adalah fisikawan Prancis Antoine-Henri Becquerel, yang memperhatikan, pada tahun 1896, tanda yang dibuat pada film fotografi oleh sampel garam uranium.
Namun, itu adalah Pasangan Curie yang pertama kali menggunakan istilah radioaktivitas. Di 1898, poles Marie Curie melanjutkan studi tentang radioaktivitas dan membuat penemuan berharga untuk daerah tersebut, seperti penemuan dua unsur radioaktif baru: polonium (Po) dan radium (Ra).
posterior, Ernest Rutherford menemukan radiasi tipe alfa (α) dan beta (β), yang memungkinkan penjelasan yang lebih baik untuk model atomnya, serta kemajuan penelitian yang berkaitan dengan radioaktivitas.
Baca juga:Marie Curie: biografi, kontribusi, dan warisan
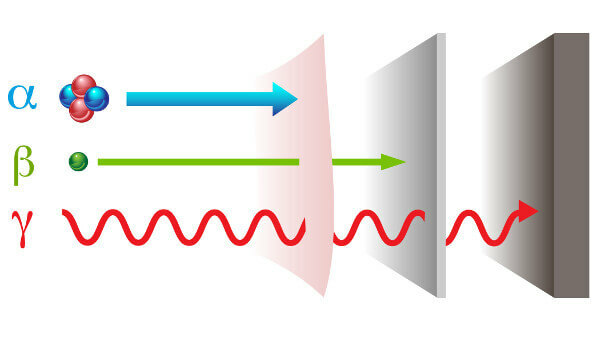
Jenis radiasi dan kekuatan penetrasinya.
kerusakan
HAI peluruhan radioaktif (atau transmutasi) adalah proses alami di mana inti tidak stabil memancarkan radiasi, berturut-turut, untuk turunkan energimu dan menjadi stabil.
Ini biasanya terjadi dengan atom nomor atom. lebih besar dari 84, yang merupakan atom dengan ketidakstabilan tinggi inti karena jumlah muatan positif (proton) yang terkumpul di dalam inti. Dalam proses ini, neutron tidak cukup untuk menstabilkan semua proton yang berkerumun di dalam nukleus, dan kemudian nukleus mulai mengalami peluruhan radioaktif hingga nomor atomnya kurang dari 84.
Dalam beberapa kasus, mungkin terjadi bahwa atom dengan nomor atom kurang dari 84 memiliki inti yang tidak stabil dan juga melalui proses peluruhan, tetapi untuk itu mereka harus memiliki jumlah proton jauh di atas jumlah neutron.
Peluruhan radioaktif adalah dihitung dengan waktu paruh (atau periode setengah hancur, P) dari radioisotop, yang merupakan waktu yang diperlukan untuk setengah massa sampel radioaktif awal untuk hancur, yaitu menjadi stabil. Secara grafis, konsep waktu paruh diwakili di bawah ini. Karena itu adalah proses berkelanjutan, kurva cenderung mencapai nol.
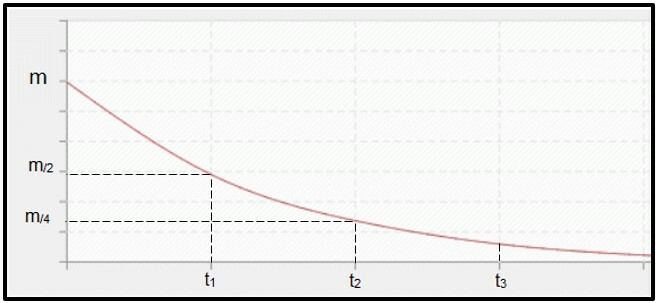
Grafik yang mewakili waktu paruh.
Perhitungan yang melibatkan peluruhan radioaktif mengikuti rumus berikut:
Rumus untuk menghitung sisa massa setelah waktu paruh:
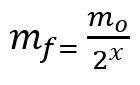
sayaf - massa akhir
sayaHAI - massa awal
x – jumlah waktu paruh yang telah berlalu
Rumus untuk menghitung waktu hancur sampel radioaktif:
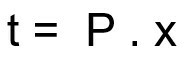
t – waktu hancur
P - waktu paruh
x – jumlah waktu paruh yang telah berlalu
unsur radioaktif
Ada dua jenis unsur radioaktif: kamu alam dan buatan. Yang alami memiliki unsur-unsur yang ditemukan di alam, sudah dengan inti yang tidak stabil, seperti uranium, O aktinium ini adalah radio. Yang buatan dihasilkan oleh proses yang mengacaukan inti atom. Dalam hal ini, kita dapat menyebutkan astatin ini adalah fransium.
Unsur radioaktif utama adalah: uranium-235, kobalt-60, strontium-90, radium-224 dan yodium-131. Karena penggunaannya yang luas dalam pembangkit listrik tenaga nuklir dan perawatan kanker, unsur-unsur ini cenderung lebih sering muncul dalam kehidupan kita sehari-hari. Untuk mempelajari lebih lanjut tentang subjek ini, kunjungi: unsur radioaktif.
Sampah radioaktif
Limbah radioaktif atau limbah nuklir ini adalah residu dari industri yang menggunakan bahan radioaktif dalam prosesnya yang tidak lagi memiliki aplikasi praktis. Sampah ini terutama berasal dari pembangkit listrik tenaga nuklir ini berasal aplikasi medis.
Besarnya produksi limbah radioaktif telah masalah lingkungan untuk seluruh dunia, karena langka dan tidak memadai and kondisi pembuangan dan penyimpanan.
Tailing ini terkait dengan kontaminasi tanah, saluran air dan udara, yang mengakibatkan perusakan lingkungan bertahap. Selain itu, mereka juga menimbulkan risiko bagi kesehatan manusia, seperti: infeksi, kanker dan, dalam kasus kontaminasi yang lebih parah, mereka dapat menyebabkan kematian.
latihan yang diselesaikan
(PUC-Camp-SP) Bom atom, juga disebut bom nuklir, memiliki atom uranium-235 sebagai penyusun fisilnya, , pemancar partikel alfa
, pemancar partikel alfa 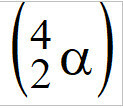 . Setiap atom U-235, ketika memancarkan partikel alfa, berubah menjadi elemen lain, yang nomor atomnya sama dengan
. Setiap atom U-235, ketika memancarkan partikel alfa, berubah menjadi elemen lain, yang nomor atomnya sama dengan
a) 231.
b) 233.
c) 234.
d) 88.
e) 90.
Templat: Ketika sebuah atom memancarkan partikel alfa, ada pengurangan dua unit dalam nomor atom, menurut hukum pertama radioaktivitas. Jadi: 92-2 = 90. Huruf e.
(PUC-Camp-SP) Iodine-125, berbagai radioaktif Yodium dengan aplikasi obat, memiliki waktu paruh 60 hari. Berapa gram yodium-125 yang tersisa setelah enam bulan, berdasarkan sampel yang mengandung 2,00 g radioisotop?
a) 1,50
b) 0,75
c) 0,66
d) 0,25
e) 0,10
Templat: Pertama, jumlah waktu paruh yang berlalu selama 180 hari dihitung:
t = P x
180 = 60. x
x = 3
Setelah jumlah waktu paruh ditemukan, massa yang tersisa pada akhir 180 hari dihitung:
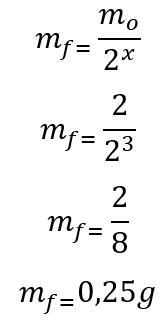
Oleh karena itu, 0,25g radioisotop Yodium-135 akan tetap ada pada akhir enam bulan. Huruf D
Oleh Victor Felix
Lulus kimia

