ITU energi aktivasi adalah jumlah energi minimum yang diperlukan untuk tumbukan antara partikel reaktan, dibuat dalam orientasi yang menguntungkan, untuk membuat dan menghasilkan reaksi.
Reaksi hanya terjadi ketika reaktan memiliki energi aktivasi (atau energi minimum yang dibutuhkan, yang bervariasi dari reaksi ke reaksi; baik dalam jumlah atau bentuk) atau ketika dipasok kepada mereka.
Misalnya, ketika logam natrium bersentuhan dengan air, ia bereaksi keras. Ini berarti bahwa kandungan energi reaktan ini sudah cukup untuk berlangsungnya reaksi.
Dalam kasus menyalakan kompor, reaksi pembakaran hanya akan terjadi jika kita meletakkan korek api yang menyala atau sumber api lain di dekat gas yang dikeluarkan oleh kompor. Artinya, dalam hal ini diperlukan suplai energi ke sistem sehingga mencapai energi aktivasi dan reaksi berlangsung.
Dalam kasus fosfor itu sendiri yang digunakan, untuk membakarnya, energi aktivasi disediakan oleh gesekan. Hal yang sama terjadi dengan korek api, yang juga membutuhkan percikan yang memberikan energi aktivasi yang diperlukan untuk pembakaran gas yang terkandung di dalamnya.
Energi aktivasi juga dapat diberikan oleh cahaya, seperti halnya dengan dekomposisi hidrogen peroksida. Itu sebabnya disimpan dalam botol gelap atau buram.
Jangan berhenti sekarang... Ada lagi setelah iklan ;)

Dengan demikian, kita dapat menyimpulkan bahwa energi aktivasi (Esampai) adalah selisih antara energi yang diperlukan untuk memulai reaksi (E) dan energi yang terkandung dalam reaktan (Epra):

Energi aktivasi merupakan penghambat berlangsungnya reaksi dan diperlukan untuk memutuskan ikatan reaktan. Dengan ini, reaksi terjadi dan koneksi baru dibuat untuk membentuk produk.
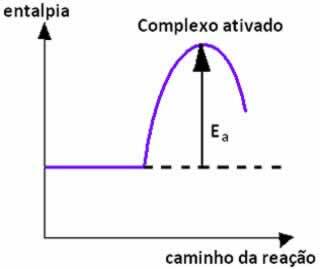
Ketika tumbukan antara partikel reaktan dengan orientasi yang menguntungkan terjadi dengan energi yang sama atau lebih tinggi dari energi aktivasi, sebelum pembentukan produk, keadaan antara dan tidak stabil terbentuk, mata uang kompleks teraktivasi, di mana ikatan reaktan melemah dan ikatan produk terbentuk. Jadi, energi aktivasi adalah energi yang dibutuhkan untuk membentuk kompleks teraktivasi.
Di bawah ini kami memiliki grafik yang menunjukkan energi aktivasi sebagai penghalang untuk berlangsungnya reaksi:
Oleh Jennifer Fogaa
Lulus kimia
Apakah Anda ingin mereferensikan teks ini di sekolah atau karya akademis? Lihat:
FOGAÇA, Jennifer Rocha Vargas. "Energi aktivasi"; Sekolah Brasil. Tersedia di: https://brasilescola.uol.com.br/quimica/energia-ativacao.htm. Diakses pada 27 Juni 2021.