Amikor a benzolgyűrűnek már van szubsztituense, ez a gyök befolyásolja a gyűrű összes többi H szubsztitúcióját. Ez a szubsztituens lehet orto és para-igazgató vagy meta-igazgató. De felmerülnek a kérdések:
| Mi okozza a benzolgyűrűhöz kötődő csoport hatását a szubsztitúciós reakció irányára és reakcióképességére? |
| Mi teszi bizonyos csoportokat céltanácsadókká (letiltva) és másokat orto-para (aktiválóvá)? |
Erre a két kérdésre ad választ a hívások megértése. elektronikus effektusok hogy ezek a csoportok a ringben gyakorolnak. Ez a hatás a elektronegativitás különbség az elemek között, ahogy a szubsztituens akarja polarizálja az aromás mag kötéseit, felváltva pozitív karaktert indukálva egyes gyűrűs szénatomokra, míg mások negatív jellegűek maradnak.
| Új szubsztitúció következik be a karakteres szénatomokban negatív. |
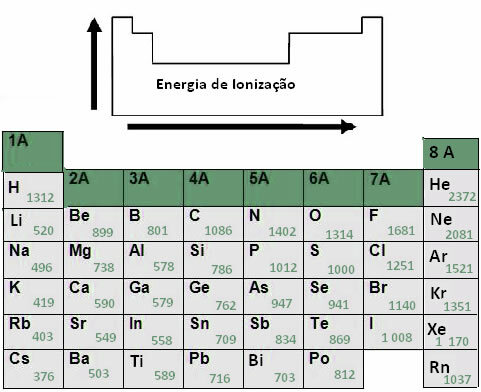
Nézzük meg, hogyan fordulnak elő ezek az elektronikus effektek az aromás gyűrűben, szem előtt tartva az elemek elektronegativitási sorrendjét: F> O> N> Cl> Br> S> C> I> H.
1. eset: Radikálisan aktiváló vagy orto-to-director:
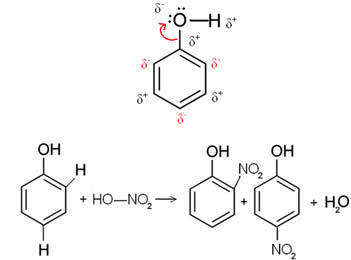
Például a benzol (fenol) molekula alatt lévő esetben az oxigén a leginkább elektronegatív elem, tehát elektronokat vonz magához, emiatt a szén részben pozitív töltéssel rendelkezik, ami indukál váltakozó gyűrűs polarizáció. A negatív pozíciók pontosan az orto és a para pozíciók. Ezért az -OH csoport egy aktiváló csoport vagy orto-to-rendezők. Ez megfigyelhető az alábbi fenol-nitrálási reakcióban, amely termékként o-nitrofenolt és p-nitrofenolt eredményez:
Ne álljon meg most... A reklám után még több van;)
2. eset: radikális vagy metavezérlő deaktiválása:
Most vegyük figyelembe a nitrobenzol esetét:
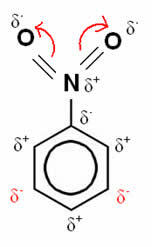
Ebben a példában az oxigén marad a legelektronegatívabb elem, így magához vonzza a nitrogénnel létrejött kötéseket, amely részben pozitív töltésű, és a hozzá kapcsolódó szénatom negatív polarizálódásra készteti, és így egymás után. Így az a helyzet, amely negatívvá válik és a leginkább fogékony a helyettesítésre, az a pozíció cél, lévén tehát a letiltása.
Lásd most részletesebben ezt az elektronikus hatást, amelyet ún rezonáns hatás.
| rezonáns hatás ez az elektronok vonzása vagy taszítása a kettős vagy hármas kötések π (pi) kötésein, amikor magával a benzolgyűrűvel rezonálnak. |
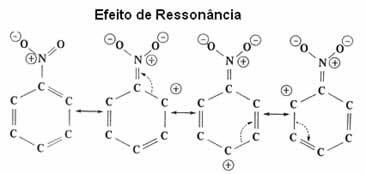
Amint látható, az NO2 csoport deaktiválja a gyűrűt, mivel elektronokat vesz ki belőle és csökkenti elektronsűrűségét. Így az a csoport, amely megtámadja és szubsztitúciót hajt végre (elektrofil), pozitív, tehát előnyösen a negatív töltést kapott meta-helyzetet fogja megtámadni.
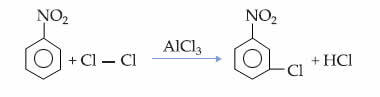
Ez a tény a nitrobenzol monoklorin-reakciójában látható, amelyben a helyettesítés csak meta-helyzetben történik:
Írta: Jennifer Fogaça
Kémia szakon végzett
Brazil iskolai csapat
Hivatkozna erre a szövegre egy iskolai vagy tudományos munkában? Néz:
FOGAÇA, Jennifer Rocha Vargas. "A meta és az orto-to-rendezők radikálisainak elektronikus hatásai"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm. Hozzáférés: 2021. június 28.