A középiskolások mindig szembesülnek redox-reakciók val vel ionok, mind a felvételi vizsgákon, mind az Országos Középiskolai Vizsgán (Enem). Így ezeknek az egyenleteknek az egyensúlyba hozása nagyon féltett téma lehet.
A téma megértésének megkönnyítése érdekében ez a szöveg a következőkkel kíván foglalkozni a redox-egyenletek kiegyenlítése az ionokkal a végrehajtásának néhány lépésével. Ehhez el kell kezdenünk az ilyen típusú kémiai reakciók azonosítását.
Nál nél redoxreakciók ionokkal - egy vagy több (pozitív vagy negatív) töltéssel rendelkező komponens jelenlétével azonosítják, vagyis a ionok (kationok vagy anionok), amelyek jelen lehetnek a reagensekben vagy termékekben, ahogy a két a kövesse:
1. példa:Kr. |2O72- + Fe2+ + H+ → Kr3+ + Fe3+ + H2O
2. példa:Cl2 + C + H2O → CO2 + H+ + Cl-
Végezni a a redox-reakciók és az ionok egyenleteinek kiegyensúlyozása elengedhetetlen néhány lépés végrehajtása, például:
1. lépés: határozzuk meg a NOX-ot a reaktánsok egyes atomjai és az egyenlet termékei;
2. lépés: ellenőrizze, melyik faj szenvedett oxidáció;
3. lépés: határozza meg a NOX az oxidáción átesett faj;
4. lépés: szorozzuk meg a harmadik lépésben talált variációt az oxidáló faj atomjainak számával;
5. lépés: ellenőrizze, melyik faj szenvedett csökkentés;
6. lépés: határozza meg a redukción átesett fajok NOX-variációját;
7. lépés: szorozzuk meg a harmadik lépésben talált variációt a faj által csökkentett atomok számával;
8. lépés: használja a negyedik lépésben talált értéket a faj együtthatójaként, amely csökkenti;
9. lépés: használja a hetedik lépésben kapott értéket az oxidáló faj együtthatójaként;
10. lépés: Helyezze az együtthatókat a többi fajba, a módszer szerint próbaegyensúlyozás. Azokban a fajokban, ahol ez nem lehetséges, ismeretleneket tegyen együtthatóvá;
11. lépés: szorozzuk meg az egyes fajok együtthatóját terhelésükkel;
12. lépés: Kiegyenlítsük a reagensek és a termékek töltésének összegét, hogy megtaláljuk az ismeretlen fajok egyikének együtthatóját;
13. lépés: Véglegesítse az egyensúlyt a próba módszerével.
A megértés megkönnyítése érdekében kövesse a fent leírt lépéseket a következő példában: a redox egyenlet ionokkal:

Ionegyenlet, amely néhány iont és általános töltéscsoportot mutat 0
1. lépés: Az egyes atomok NOX-értéke.

Az egyenletben jelen lévő atomok NOX-értéke
2. lépés: Oxidálódó fajok.

Az egyenletben oxidáción áteső fajok
Mivel a jód NOX-értéke reagenstől termékre -1-ről 0-ra nő, ezért a faj oxidálódik.
3. lépés: Határozza meg az oxidált fajok NOX-variációját.
Ehhez csak vonja le a legmagasabb NOX-ot a legalacsonyabb NOX-tal:
∆NOX = (0) – (-1)
∆ NOX = 0 + 1
∆ NOX = 1
4. lépés: A NOX szorzata mennyiséggel.
Ebben a lépésben megszorozzuk a harmadik lépésben talált variációt a faj atomjainak számával.
én- = ∆NOX.1
én- = 1.1
én- = 1
5. lépés: A redukción átesett fajok.

Az egyenlet csökkenését szenvedő fajok
Mivel a króm-NOX a reagensről a termékre +7-ről +3-ra csökken, ezért éppen ez a faj éri el a redukciót.
6. lépés: Határozza meg a redukált fajok NOX-variációját.
Ehhez csak vonja le a legmagasabb NOX-ot a legalacsonyabb NOX-tal:
∆NOX = (+6) – (+3)
∆ NOX = +6 – 3
∆ NOX = 3
7. lépés: A NOX szorzata mennyiséggel.
Ebben a lépésben megszorozzuk a hatodik lépésben talált variációt a faj atomjainak számával.
Kr. |2O72- = ∆NOX.1
Kr. |2O72- = 3.2
Kr. |2O72- = 6
8. lépés: Kezdje el az egyensúlyt.
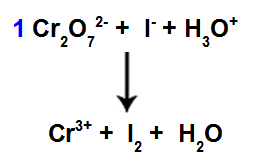
A kiegyensúlyozás kezdete a megtalált együttható alkalmazásával
Ebben a lépésben a kiegyensúlyozást azzal kezdjük, hogy a negyedik lépésben talált együtthatót helyezzük a csökkentést szenvedett fajokba.
9. lépés: Folytassa az egyensúlyozást.

Az egyensúlyozás folytatása a megtalált együttható alkalmazásával
10. lépés: Használja a próbamódszert.
A reaktánsban 6 I atom található, ezért a 3 együtthatót az I fajba kell tennünk2 a termék, mert csak 2 Cl atom van benne;
Mint az 1. fajnál, Kr2O72-, van 2 Cr-atom, a 2-es együtthatót a Cr-fajokba kell tennünk3+ termék.
Mivel három fajban van oxigénünk, és kettő közül nincsenek együtthatók, az egyensúly folytatásához ismeretleneket kell elhelyeznünk a fennmaradó fajokban:
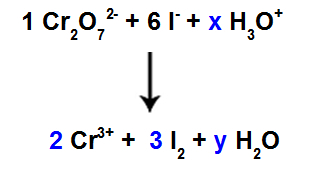
Együtthatók a vizsgálati módszer alkalmazása után
11. lépés: Minden faj szorzata terhelésével.
Ehhez csak meg kell szorozni a faj együtthatóját a terhelésével, az alábbiak szerint:
A reagensekben:
Kr. |2O72- = 1.(-2) = -2
én- = 6.(-1) = -6
H3O+ = x. (+ 1) = + x
A termékeken:
Kr. |3+ = 2.(+3) = +6
én2 = 4.0 = 0
H2O = y.0 = 0
12. lépés: A díjak összege.
Ebben a lépésben hozzá kell adnunk a 11. lépésben található reagensek és termékek mennyiségét:
Reagensek = termékek
-2 + (-8) + (+ x) = +6 + 0 + 0
-2 - 6 + x = 6
-8 + x = 6
x = 6 + 8
x = 14
13. lépés: Az egyensúlyozás vége.
Az egyensúlyozás befejezéséhez:
Tedd a 12. lépésben kapott eredményt a H fajba3O+;
Mivel 42 reagensünk van a reagensben, a 21-es együtthatót a H-fajba kell helyezni2A termékben.
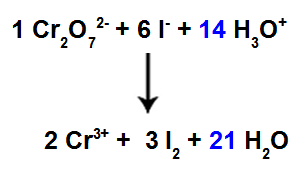
Kiegyensúlyozott ionos reakcióegyenlet
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao-com-ions.htm

