Az anyag (atom) felépítésével kapcsolatos elképzelések az ókori Görögországban, Kr. E. 450 körül merültek fel. a., főleg a Democrito és a Leucipo-ból. Az atom azonban valójában csak azután kapott tudományos jelleget, hogy az ún Dalton atomelmélete.
A Dalton atomelmélete alapvető fontosságú volt az atomtudás fejlesztése szempontjából, mivel más tudósok alapjául szolgált az atom és jellemzőinek megismeréséhez.
Ki volt John Dalton?
John Dalton, képzett vegyész, 1766-ban született az angliai Cumbria-ban és 1844-ben Manchesterben halt meg. Élete már kicsi korától kezdve tudományos kutatás és tanítás volt, olyannyira, hogy tanított, vagy hozzájárult az ismeretek különböző területeinek fejlődéséhez.
A legnagyobb öröksége tudósként azonban az első atomelmélet kidolgozása volt. Számos, a gázkeverékkel és a Lavoisier által javasolt munkák ismeretével kapcsolatos kísérlet révén alakult ki Dalton atomelmélete 1808-ban.
Dalton atomelméletének posztulátumai
Dalton atomelmélete kísérleteken alapult, de ezek közül a kísérletek egyike sem tudta egyértelműen feltárni az atomot. Ezért Dalton az atomot az anyag legkisebb részének nevezte.
Dalton elmélete sokkal több posztulátumot mutat be, mint bizonyítást. Tekintsen meg néhányat közülük:
Az atomok masszívak és gömb alakúak (hasonlóak a biliárd labdához);
Az atomok oszthatatlanok;
Az atomok elpusztíthatatlanok;
Egy kémiai elem ez ugyanazokkal a tulajdonságokkal (méret és tömeg) rendelkező atomok halmaza;
A különböző kémiai elemek atomjainak tulajdonságai eltérnek egymástól;
Két atom relatív súlya megkülönböztethető;
Az összetett vegyi anyagokat különböző típusú atomok azonos kombinációja képezi;
Különböző kémiai anyagok keletkeznek a különböző atomok kombinálásával.
A Dalton Atomic Model ábrázolásai
Dalton atomi modelljét a biliárdgolyónak nevezte el, ezért gömb alakú szimbólumok segítségével kezdte képviselni a korában ismert elemek atomjait.
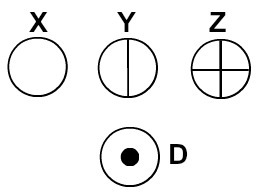
Dalton atomelmélete szerint képviselt atomok
Minden atomi reprezentáció, amelynek egy adott részlete van, más kémiai elemet jelöl. Didaktikailag az elemi és a középszintű könyvek és gyakorlatok csak különböző színű gömbökön keresztül reprezentálják az atomokat.
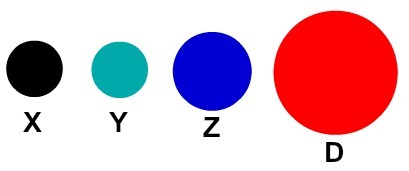
Az atomok didaktikai ábrázolása
Dalton atomelméletének közreműködései
megértése Lavoisier-féle misefenntartási törvény
Lavoisier francia vegyész 1785-ben azt állította „Egy kémiai reakció során a tömeg konzerválódik, mert nincs sem atom létrehozás, sem pusztulás ”. Dalton atomelmélete bebizonyította ezt a tényt, mivel egyik posztulátuma szerint az atom elpusztíthatatlan.
Ezért, ha a szén (C) elégetését oxigéngáz (O2), kémiai reakciónk lesz egy szénatom és két oxigénatom között. Ez a reakció szén-dioxidot (CO2), amely pontosan ugyanazokkal az atomokkal rendelkezik, mint amelyek a reakció előtt alkották az anyagokat.
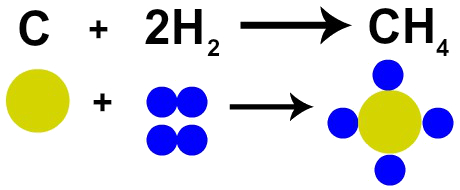
Lavoisier törvényének ábrázolása Dalton atommodelljével
megértése egyszerű anyagok
Használni a Dalton atommodellje, megérthetünk egy egyszerű anyagot, vagyis olyat, amelynek azonos tulajdonságú atomjai molekulát alkotnak. Ezért vannak atomjaink, amelyek ugyanahhoz a kémiai elemhez tartoznak.
Az F anyagban2például két fluoratomunk van, ezért az ábrázolásban kétféle egyenlő atomot kell használnunk Dalton atomelméletének megfelelően.

Egyszerű anyagábrázolás a szerint Dalton atommodellje
megértése összetett anyagok
Egy összetett anyagban különböző tulajdonságokkal rendelkező atomok alkotják a molekulát. Ezért különböző kémiai elemek alkotják az anyagot.
H anyag2Az O-nak például három atomja van: két hidrogén és egy oxigén. Lásd az ábrázolását a Dalton atommodell szerint:
Összetett anyag ábrázolása a bőr szerintDalton atommodellje
A keverékek megértése
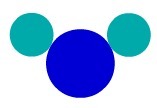
A keverék (két vagy több különböző anyag egyesülése) megértése Dalton atomelméletén keresztül egyszerű: csak két különböző molekulát kell ugyanabba a tartályba helyezni.

Egy második keverék ábrázolása Dalton atommodellje
John Dalton egyéb tudományos közreműködései
bevezette a atomtömeg;
Megfogalmazta a gázok részleges nyomásának törvényét (Dalton törvénye);
Felfedezte a látásromlást színvakság;
Tanulmányozta a gőzök és gázok viselkedését különböző hőmérsékleteken;
Megállapította, hogy minden gáz ugyanúgy tágul (megpróbálnak egy bizonyos helyet elfoglalni) a térben.
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/teoria-atomica-dalton.htm

