szervetlen sók legalább egy (bármely fémből vagy ammóniumból álló) kation és egy (egyszerű vagy vegyület) anion ionos asszociációjával jönnek létre.
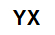
Egy só általános molekulaképlete
Vízhez adva a sók disszociálnak, és a hidroniumtól (H+) és a hidroxidtól eltérő anion (OH-).
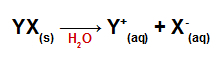
Diszociációs egyenlet bármely sóhoz
A sók osztályozása
A sók általában a következő osztályozásokba sorolhatók:
egyszerű só: só, amelyet csak egy kation és egy anion képez. Példák: NaCl, CaSO4, KCN, NH4CO3 stb.
Hidrogénezett só: két kationja van (az egyiknek hidroniumnak kell lennie) és egy anion. Példák: NaHCO3, CaHBO3 stb.
Hidroxil-só: kationja és két anionja van (az egyiknek a hidroxidnak kell lennie). Példák: MgOHCl, Al (OH)2ClO3 stb.
Hidratált só: bemutatja a kristályos szerkezetéhez kapcsolódó vízmolekulákat. Példák: CaCl2.2H2O, CuSO4.6H2Stb.
Kettős só: két kationja van (mindegyik különbözik a hidroniumtól) és egy anion vagy egy kation és két anion (mindegyik különbözik a hidroxidtól). Példák: Típus4CN, AgFeBO3 stb.
Timsó: az a só, amelyet két szulfát képez, NOx-kationokkal, amelyek egyenlőek +1 és +3, plusz 24 molekula víz. Példák: Ag
2CSAK4.Al2(CSAK4)3.24H2rajta2CSAK4.Sb2(CSAK4)3.24H2O
Só elnevezési szabály
Anion neve + de + kation neve
→ K3POR4
A só foszfátanionja (PO4-3) és a kálium-kation (K+1), ezért neve kálium-foszfát.
→ Eset3
A só szulfitanionja (SO3-2) és a kalcium-kation (Ca+2), ezért neve kalcium-szulfit.
JEGYZET: Ha a kation nem ezüst, cink vagy az IA, IIA és IIIA családokba tartozó elem, akkor a kation neve előtt római számmal kell feltüntetni annak NOX-ját.
→ Cu2CSAK4
A sóban van a szulfátanion (SO4-2) és a kalcium-kation (Cu+1), ezért neve réz-szulfát I.
Hidrogénezett só: Ehhez a sóhoz az anionnév elé kell írnunk az előtagot, amely a hidrogén mennyiségére utal a képletben. Ennek az előtagnak külön kell lennie a szótól hidrogén kötőjellel.
→ NaHCO3
A só hidrogén-, karbonát-anion- és nátrium-kationt tartalmaz, ezért neve nátrium-monohidrogén-karbonát.
Hidroxil-só: Ehhez a sóhoz az anion neve elé be kell írnunk az előtagot, amely a képletben szereplő hidroxilok mennyiségére utal. Ennek az előtagnak külön kell lennie a szótól hidroxilcsoport kötőjellel.
→ Al (OH)2ClO3
A sónak két hidroxilcsoportja van, a klorát-anion és az alumínium-kation, ezért neve alumínium-dihidroxi-klorát.
Hidratált só: Ehhez a sóhoz a kation neve után a képletben a vízmolekulák mennyiségére utaló előtagot kell írnunk. Ennek az előtagnak külön kell lennie a szótól hidratált kötőjellel.
→ CaCl2.2H2O
A sónak két vízmolekulája van, a klorid-anion és a kalcium-kation, ezért neve kalcium-klorid-dihidrát.
Kettős só két kationnal: Ehhez a sóhoz zárójelbe kell írnunk a kettős szót az anionnév után, majd a legelektropozitívabb kationnevet és a másik kationt.
→ AgFeBO3
Ez a só a borát-anion mellett ezüstöt (több elektropozitív kationt) és vas-II kationt tartalmaz. Neve borát (kettős) ezüstből és vasból II.
-
Kettős só két anionnal:
A legtöbb elektronegatív anion neve + kötőjel + a legkevésbé elektronegatív anion neve + de + kation neve
→ típus4CN
Ez a só a titán IV kationt tartalmazza a foszfát (több elektronegatív anion) és a cianid anion mellett. Neve titán-cianid-foszfát IV.
Alumsó: Ennél a sónál figyelmen kívül hagyjuk az általános szabályt. Csak írja be a timsó kifejezést, majd a +3 töltéskation nevet és a +1 töltéskation nevet, e-vel elválasztva.
→ Be2CSAK4.Sb2(CSAK4)3.24H2O
A timsó sójának +3 antimonkationja és +1 nátriumkationja van, ezért neve antimon III timsó és nátrium.
A sók fizikai jellemzői
Szobahőmérsékleten szilárdak;
Magas olvadás- és forráspontjuk van;
Ionkötésekből képződnek;
Folyékony állapotban vezetnek elektromos áramot (fúzió után) vagy vízben oldva;
Általánosságban elmondható, hogy vízben oldódnak, de vannak sók, amelyeket gyakorlatilag oldhatatlannak tartanak.
A sók kémiai tulajdonságai
A sók olyan vegyületek, amelyek képesek kémiailag reagálni (feltéve, hogy nem ugyanaz a kation vagy ugyanaz az anion, mint egy másik anyag) több anyagcsoporttal, nevezetesen:
Savval végzett kettős cserereakcióban: új sót és új savat képeznek.
Bázissal végzett kettős cserereakcióban: új sót és új bázist alkotnak.
A kettős csere reakció egy másik sóval: két új sót képez.
Egyes sók képesek szenvedni bomlás ha hő hatására két vagy több új anyag képződik. Ha a nátrium-hidrogén-karbonátot (NaHCO3), például lebomlik, nátrium-karbonátot (Na2CO3), víz (H2O) és szén-dioxid (CO2).
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-sais-inorganicos.htm