A kovalens kötés akkor következik be, amikor két atom megosztja az elektronpárokat annak érdekében, hogy megszerezzék az elektron elektronkonfigurációját nemesgáz (8 elektronnal a vegyértékes héjban vagy 2-vel, azok esetében, amelyeknek csak a K-héja van), a szabály szerint oktett.
Vannak azonban olyan kovalens kötések speciális esetei, amelyekben a megosztott elektronpár csak az egyik atomból származik, amely már stabil. Korábban ezt a típusú kovalens kötést hívták részeshatározó, ma már gyakrabban hívják koordináta.
Néhány példa a megértéshez:
- CO (szén-monoxid):
A szén vegyértékhéjában 4 elektron van. Ezért az oktett szabály szerint ahhoz, hogy stabil legyen, további 4 elektront kell fogadnia, összesen 8-at. Az oxigénnek viszont 6 elektronja van a vegyértékhéjban, és 2 elektron befogadására van szüksége a nemesgáz neon konfigurációjának megszerzéséhez.
Tehát először a szénnek és az oxigénnek két elektronpárja van, így az oxigén stabil:
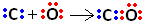
A szén azonban instabil marad, mivel még mindig 6 elektronja van, és 2-re van szüksége. Ezért az oxigén, amely már stabil, megosztja az egyik elektronpárját a szénnel, vagyis dátumkötést létesít vele, így stabil lesz:

Ne feledje, hogy a koordinátás kovalens kötés kötőjellel ábrázolható, akárcsak a közös kovalens kötés.
- CSAK2 (Kén-dioxid):
Valamennyi kén- és oxigénatomnak 6 elektronja van a vegyértékhéjában, ezért egyenként 2 elektront kell befogadniuk. Kezdetben a kén két közös kovalens kötést hoz létre, két elektronpárt oszt meg az oxigénatomok egyikével, mindkettő 8 elektron mellett stabil marad.
De a másik oxigénatom nem stabil, ezért a kén összehangolt vagy datatív kovalens kötésen keresztül osztja meg vele pár elektronját:
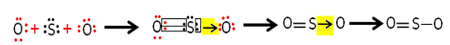
Megjegyezzük, hogy ebben az esetben a molekulában három atom van, így a kötés egyik atomról a másikra vándorolhat. A kén-dioxid molekula így is ábrázolható: O ─ S ═ O.
Ezt a kötődési jelenségnek hívjuk rezonancia. További három példát lásd az alábbi táblázatban:
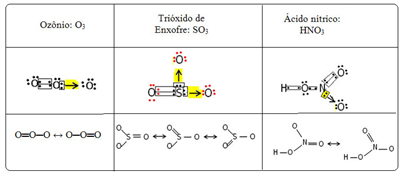
A lehetséges struktúrákat hívjuk rezonancia struktúrák vagy kanonikus formák.
Ez a kötéstípus ionok képződésében is előfordul, akárcsak a hidroniumionok (H3O+) és ammónium (NH4+).
Először a H kation+ akkor keletkezik, amikor a hidrogén elveszíti egyetlen elektront, és pozitív töltéssel rendelkezik. Tehát két elektron fogadására van szükség ahhoz, hogy stabil legyen. Ez a vízzel (a hidroniumion esetében) és az ammóniával (az ammóniumion esetében) való kötődés révén történik. Néz:

Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/ligacao-covalente-dativa-ou-coordenada.htm

