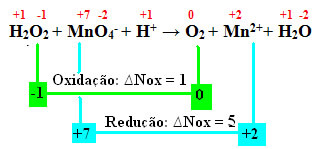
AZ oxidáció és a csökkentés olyan reakciók, amelyek akkor lépnek fel, amikor a elektrontranszfer kémiai fajok között. Ellentétes reakciók: az oxidációban elektronveszteség, redukcióban pedig elektronnövekedés következik be.
Ezek a folyamatok egyszerre mennek végbe, mert amikor egy anyag elektronokat ad át egy másiknak, az oxidálódik, míg az elektronokat fogadó anyag redukción megy keresztül.
Amikor egy anyag oxidálódik, a többi faj redukcióját okozza, innen ered a redukálószer elnevezés. Hasonlóképpen, az egyik anyag a másik oxidációja miatt redukálódik, és ezért oxidálószer.
Az oxidációs és redukciós reakciókat az érintett fajok oxidációs számának (nox) változása mutatja.
Általában az oxidációt és redukciót mutató reakció a következőképpen ábrázolható:
A + B+ → A+ + B
Ahol,
V: Olyan anyag, amely oxidálódik, elektronokat veszít, növeli értékét és redukálószer.
B: olyan anyag, amely redukción megy keresztül, elektronokat nyer, csökkenti az oxidációt és oxidálószer.
Példák oxidációra és redukcióra
Lásd a következő képet a redox kémiai egyenlet példájához.
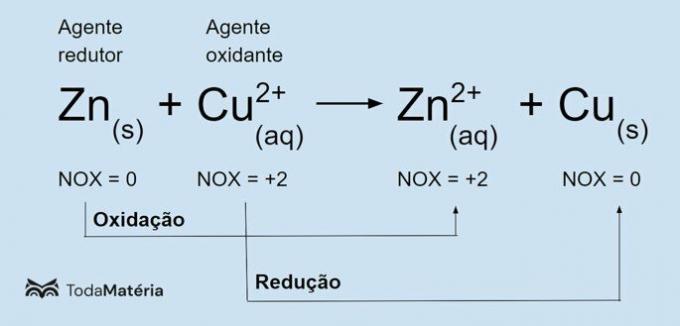
A fémes cink átmegy oxidáció és a réz redukcióját okozza, tehát redukálószer. Oxidációs száma (nox) 0-ról +2-re nő, mert 2 elektront veszít.
A rézion (Cu2+) redukción megy keresztül, és a réz oxidációját okozza, így ez az oxidálószer. Oxidációs száma (nox) +2-ről 0-ra csökken, mert 2 elektront nyer és fémes réz lesz, ami elektromosan semleges.
További példák a redox reakciókra a mindennapi életben:
metán égetése
CH4(g) + 2O2(g) → CO2(g) + 2H2O(v)
Fotoszintézis
6CO2(g) + 6H2O(v) → C6H12O6 (itt) + 6O2(g)
vaskorrózió
2Fe(s) + 3/4O2(g) + 3 óra2O(v) → 2Fe (OH)3(s) (rozsda Fe2O3.3H2O)
Tudj meg többet oxidációs szám (nox).
Hogyan mennek végbe az oxidációs és redukciós reakciók?
A réz és a cink redoxreakciójának egyenlete félreakciókkal ábrázolható, az alábbiak szerint.
- oxidációs félreakció: Zn0(s) → 2e- + Zn2+(itt)
- Félreakció csökkentése: szamár2+(itt) + 2e- → szamár0(s)
- globális egyenlet: Zn0(s) + szamár2+(itt) → Zn2+(itt) + szamár0(s)
Ez az elektrontranszfer a redoxreakcióban az érintett faj redukciós potenciálja szerint megy végbe. A legalacsonyabb redukciós potenciállal rendelkező komponens hajlamos elektronokat adni, míg a legnagyobb potenciállal rendelkező komponens fogadja azokat.
Például a cink redukciós potenciálja -0,76 V, míg a réz redukciós potenciálja +0,34 V. Ezért a cink, mivel alacsonyabb redukciós potenciállal rendelkezik, jobb redukálószer és elősegíti a redukciót réz, amelynek nagyobb a redukciós potenciálja, ezért elektronokat nyer, és cinkoxidációt okoz.
Olvass még róla redox reakciók.
Oxidációs és redukciós gyakorlatok
Használja a következő kérdéseket, hogy tesztelje tudását az ebben a szövegben tanultakról.
1. kérdés
Az oxidációs és redukciós reakciókkal kapcsolatban helyénvaló azt állítani
a) A kémiai fajok nox-értékének növekedése azt jelzi, hogy csökkenésen ment keresztül.
b) Az elektronokat veszítő anyag oxidáción megy keresztül, és oxidálószer.
c) Redox reakciókban elektronok átvitele történik.
d) Az elektronokat nyerő anyag redukálódik és redukálószer.
e) A kémiai anyagfajták nox-értékének csökkenése azt jelzi, hogy oxidáción ment keresztül.
Helyes alternatíva: c) Az oxidációs-redukciós reakciókban elektrontranszfer megy végbe.
A redox reakciókban elektronok átvitele történik meg.
Az elektronokat nyerő anyag redukción megy keresztül, és oxidálószer. A kémiai fajok nox-értékének csökkenése azt jelzi, hogy csökkent.
Az elektronokat veszítő anyag oxidáción megy keresztül, és redukálószer. A vegyi anyagok nox-értékének növekedése azt jelzi, hogy oxidáción ment keresztül.
2. kérdés
Példák redox reakciókra a mindennapi életben KIVÉVE
a) Korrózió
b) égés
c) Fotoszintézis
d) Semlegesítés
Helytelen alternatíva: d) Semlegesítés.
A semlegesítési reakció sav és bázis között megy végbe, és sót és vizet eredményez. Például:
NaOH + HCl → NaCl + H2O
Példák a redox reakcióra:
metán égetése
CH4(g) + 2O2(g) → CO2(g) + 2H2O(v)
Fotoszintézis
6CO2(g) + 6H2O(v) → C6H12O6 (itt) + 6O2(g)
vaskorrózió
2Fe(s) + 3/4O2(g) + 3 óra2O(v) → 2Fe (OH)3(s)
3. kérdés
Figyelje meg a következő oxidációs-redukciós reakciókat, és jelölje meg, melyek az oxidáló- és redukálószerek.
ÉN. Zn0(s) + szamár2+(itt) → Zn2+(itt) + szamár0(s)
II. Szamár2+(itt) + H2(g) → 2H+(itt) + szamár(s)
III. Zn(s) + 2H+(itt) → Zn2+(itt) + H2(g)
Válasz:
A redox reakcióban az oxidáción átmenő a redukálószer, a redukción átmenő pedig az oxidálószer.
ÉN. Zn0(s) + szamár2+(itt) → Zn2+(itt) + szamár0(s)
Oxidálószer: réz (Cu)
Redukálószer: cink (Zn)
II. Szamár2+(itt) + H2(g) → 2H+(itt) + szamár(s)
Oxidálószer: réz (Cu)
Redukálószer: hidrogén (H)
III. Zn(s) + 2H+(itt) → Zn2+(itt) + H2(g)
Oxidálószer: hidrogén (H)
Redukálószer: cink (Zn)
Szerezzen további ismereteket a tartalommal:
- Mik azok a veremek?
- elektrokémia
- Elektrolízis
Bibliográfiai hivatkozások
FONSECA, M. R. M kémia, 2. 1. szerk. São Paulo: Attika, 2013.
SANTOS, W.L.P; MOL, G.S. Polgári kémia, 3. 2. szerk. São Paulo: AJS szerkesztő, 2013.
USBERCO, J. Connect kémia, 2: kémia. - 2. szerk. São Paulo: Saraiva, 2014.