Párolgás ez a folyékony állapotból a gáz halmazállapotba való átjutás. A folyadékok szabad felületén, lassan és fokozatosan, bármilyen hőmérsékleten fordul elő.
Ha egy anyag folyékony állapotban van, akkor kisebb az összetartó ereje az atomjai között, mint amikor szilárd állapotban van.
Ebben az állapotban a molekulák egymástól távolabb vannak, állandó keverés alatt állnak, és különböző sebességgel mozognak a folyadék belsejében.
Ily módon a részecskék nagyobb sebességgel, a folyadék szabad felületének elérésekor, képesek elmenekülni, gáznemű állapotba kerülve.

Párolgási sebesség
Vannak olyan tényezők, amelyek befolyásolják a párolgás sebességét, ezek:
- Hőfok: minél magasabb a hőmérséklet, annál gyorsabb a párolgási sebesség. Mivel minél magasabb a hőmérséklet, annál magasabb a kinetikus energia a részecskék. Ily módon több részecske távozik a folyadék felületéről.
- A folyadék jellege: vannak olyan anyagok, amelyek könnyebben elpárolognak, illékony anyagoknak hívják őket. Az éter, az alkohol és az aceton az illékony anyagok példái.
- szabad felület: mivel a párolgás a folyadékok szabad felületén megy végbe, minél nagyobb a felület, annál nagyobb a részecskék mennyisége, amely elhagyja a folyadékot.
- A gőz koncentrációja folyadékon: minél nagyobb a gőzmennyiség, annál alacsonyabb a párolgási sebesség.
- A folyadékra gyakorolt nyomás: minél nagyobb a nyomás, annál kisebb a párolgási sebesség.
Különbség a párolgás és a forralás között
Párologtatás és forró képviselik a folyékony állapotból a gáz halmazállapotba történő változást. Míg a párolgás fokozatosan megy végbe, a forralás gyorsan megtörténik.
A forraláshoz szükséges, hogy a folyadék adott nyomáson elérjen egy bizonyos hőmérsékletet, az úgynevezett forráspontot. Párolgás bármely hőmérsékleten előfordulhat.
Keverékek elválasztása
A frakcionált kristályosítás heterogén keverékek elválasztásának folyamata. Akkor alkalmazzák, ha a keveréket alkotó anyagok szilárd állapotban vannak.
Ebben a folyamatban az összes szilárd komponenst feloldó folyadékot adunk a keverékhez. A komponensek az oldat elpárolgása után külön-külön kristályosodnak.
Ezt az eljárást alkalmazzák például sótartályokban sók kinyerésére tengervízből.

Párolgás és a vízciklus
A párolgás az egyik folyamat, amely a a víz körforgása. A Napból származó energia felmelegíti a tavak, folyók, tengerek és óceánok szabad felületét.
Ez a melegítés a víz egy részének gőzállapotba kerülését eredményezi. Ez a légkör legmagasabb rétegeire jutva hűl és kondenzálódik, felhőket képezve.
A csapadék bekövetkezésekor a víz folyékony formában tér vissza a felszínre, beszivárog a talajba, és föld alatti lapokat képez.
Ennek a víznek egy részét elnyelik a növények, amelyek transzpirációval visszajuttatják a vízgőzt a légkörbe.
fázisváltozások
A folyékony állapotból a gáz halmazállapotúvá válást általában hívják párologtatás, mivel a párolgás mellett két másik folyamatot is magában foglal: a forralást és a melegítést.
Az államváltásnak még vannak más folyamatai. Vannak:
- Fúzió
- Megszilárdulás
- Cseppfolyósítás vagy kondenzáció
- Szublimáció
Az alábbi ábrán a hármat ábrázoljuk az anyag fizikai állapota és a vonatkozó állapotváltozások:
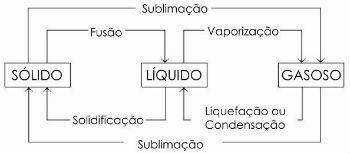
További információ itt:: Fizikai állapotváltozások.