A kémiai egyensúly az egyik olyan tárgy, amely leginkább esik az Enem és a felvételi vizsgákra.
A reverzibilis reakciók szempontjaival a kérdések foglalkoznak, és a jelentkezőket mind számításokkal, mind az e témát magában foglaló koncepciókkal értékelik.
Ezt szem előtt tartva készítettük ezt a kérdéslistát a kémiai egyensúly eltérő megközelítésével.
Használja a felbontással kapcsolatos megjegyzéseket a vizsgákra való felkészüléshez, és olvassa el a kérdések megoldásának lépésenkénti útmutatásait.
A kémiai egyensúly általános fogalmai
1. (Uema) Az egyenletben , a kémiai egyensúly elérése után következtethetünk az egyensúlyi állandóra
, amelyről helyes kijelenteni, hogy:
a) minél nagyobb a Kc értéke, annál alacsonyabb a közvetlen reakció hozama.
b) Kç hőmérséklettől függetlenül.
c) ha az előre- és az inverz reakció sebessége megegyezik, akkor Kc = 0.
d) Kç a reagensek kezdeti molaritásától függ.
e) minél nagyobb a Kc értéke, annál nagyobb a termékek koncentrációja.
Helyes válasz: e) minél nagyobb a Kc értéke, annál nagyobb a termékek koncentrációja.
A közvetlen reakciót az 1. szám jelöli, ahol:
Az inverz reakciót a
K értékeç a termékek és a reagensek koncentrációinak aránya alapján számítják ki.
A számláló (amely a szorzatokat tartalmazza) egyenesen arányos az egyensúlyi állandóval. Ezért minél magasabb a K értékeç, annál nagyobb a közvetlen reakció hozama, mivel több termék képződik, és ennek következtében annál nagyobb a termékek koncentrációja.
K értékeç a hőmérséklettől függően változik, mert amikor megváltoztatjuk az értékét, az endoterm (hőelnyelő) vagy az exoterm (hőfelszabadító) reakció bekövetkezhet előnyösebb, és ezzel több reagens vagy termék fogyasztható vagy hozható létre, megváltoztatva ezzel az egyensúlyi állandót, amely a reagensek.
A Kc az összetevők moláris mennyiségétől függ, ha egyensúly alakul ki, és ha az előre- és a fordított reakció sebessége azonos.
2. (UFRN) A kémiai egyensúlyt az jellemzi, hogy mikroszkopikus szinten dinamikus. A kémiai egyensúly mértékére vonatkozó kvantitatív információk megszerzéséhez az egyensúlyi állandó mennyiséget használjuk. Vegye figyelembe a következő csíkot:

A kémiai egyensúlyra alkalmazva a karakter egyensúly-ötlete:
a) Helyes, mert a kémiai egyensúlyban a mennyiség fele mindig termék, a másik fele pedig reagens.
b) Nem helyes, mivel a kémiai egyensúlyban a termékek és a reagensek koncentrációja eltérő lehet, de állandó.
c) Helyes, mert a kémiai egyensúlyban a reagensek és a termékek koncentrációi mindig megegyeznek, amennyiben az egyensúlyt nem zavarja külső hatás.
d) Nem helyes, mivel a kémiai egyensúlyban a termékek koncentrációja mindig magasabb, mint a reagenseké, mindaddig, amíg az egyensúlyt nem befolyásolja külső tényező.
e) Helyes, mert a kémiai egyensúlyban a reagensek és a termékek koncentrációja nem mindig azonos.
Helyes válasz: b) Nem helyes, mivel a kémiai egyensúlyban a termékek és a reagensek koncentrációja eltérő lehet, de állandó.
Egyensúly esetén a termékek és reagensek mennyisége kiszámítható a egyensúly, és nem feltétlenül a termékmennyiség felének, a másik felének kell lennie reagensek.
Az egyensúlyi koncentrációk nem mindig azonosak, eltérőek lehetnek, de állandóak, ha az egyensúlyban nem fordulnak elő zavarok.
Az egyensúlyi koncentrációknak attól kell függeniük, hogy melyik reakciót részesítik előnyben, legyen az közvetlen vagy fordított. Ezt a K értéke alapján ismerhetjük megç: ha Kç 1, a közvetlen reakciót részesítik előnyben. már ha Kç
1 a fordított reakciót részesítik előnyben.
Kémiai mérlegdiagramok
3. (UFPE) A 20. század elején az első világháború várakozása nagy szükségletet generált a nitrogénvegyületekre. Haber úttörő szerepet játszott az ammónia nitrogénből történő előállításában a levegőben. Ha az ammóniát zárt tartályba helyezzük, az a következő kiegyensúlyozatlan kémiai egyenlet szerint bomlik: NH3g) → N2. g) + H2. g). A koncentrációk időbeli változásait a következő ábra szemlélteti:

A fenti ábra elemzéséből megállapíthatjuk, hogy az A, B és C görbék a következő reakciókomponensek koncentrációinak időbeli változását jelentik:
a) H2, nem2 és NH3
b) NH3, H2 és nem2
c) NH3, nem2 és H2
d) Nem2, H2 és NH3
e) H2, NH3 és nem2
Helyes válasz: d) N2, H2 és NH3.
1. lépés: egyensúlyozza a kémiai egyenletet.
2 NH3g) → N2. g) + 3 H2. g)
A kiegyensúlyozott reakcióval rájöttünk, hogy 2 mol ammónia szükséges nitrogénné és hidrogénné bomlani. A reakcióban keletkező hidrogén mennyisége háromszor nagyobb, mint az ammóniaé.
2. lépés: értelmezze a diagram adatait.
Ha az ammónia bomlik, akkor a grafikonon a koncentrációja a legnagyobb és csökken, ahogy a C görbe látható.
A képződő termékek a reakció kezdetekor a koncentráció nulla és növekszik, amikor a reagens termékké válik.
Mivel az előállított hidrogén mennyisége háromszor nagyobb, mint a nitrogéné, akkor ennek a gáznak a görbéje a legnagyobb, amint azt a B.
A másik képződő termék a nitrogén, amint azt az A görbe mutatja.
4. (Cesgranrio) Az egyenlet által képviselt rendszer egyensúlyban volt. Az egyensúlyi állapotot hirtelen megváltoztatta a G anyag hozzáadása. A rendszer reagál az egyensúly helyreállítására. Az alábbi diagramok közül melyik reprezentálja a legjobban a leírt folyamat során bekövetkezett változásokat?
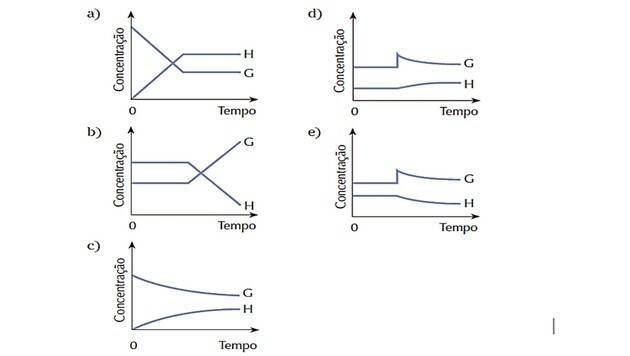
Helyes válasz: d).

Mivel a rendszer kezdetben egyensúlyban volt, a G és H anyagok mennyisége állandó maradt.
A zavar a G koncentrációjának növekedésével következett be, és a rendszer ennek átalakításával reagált reaktáns több H termékben, az egyensúly jobbra tolása, vagyis a reakció elősegítése közvetlen.
Megfigyeljük, hogy a G reagensgörbe csökken, miközben elfogyasztja, és a H termékgörbe növekszik, amikor kialakul.
Új egyensúly kialakulásakor a mennyiségek ismét állandóvá válnak.
Egyensúlyi állandó: a koncentráció és a nyomás kapcsolata
5. (UFRN) Tudva, hogy KP = Kç (RT)n, elmondhatjuk, hogy KP = Kç,
acél-2g) + H2. g) ↔ COg) + H2Og)
b) H2. g) + ½ a2. g) ↔ H2O(1)
c) Nem2. g) + 3 H2. g) ↔ 2 NH3g)
d) NEMg) + ½ O2g) ↔ NEM2g)
e) 4 FeSs + 7 O2. g) ↔ 2 Fe2O3 (s) + 4 SO2g)
Helyes válasz: a) CO2g) + H2. g) ↔ COg) + H2Og)
K-hozP egyenlő legyen K-valç az anyajegyek számának változása nulla, mivel bármely nullára emelt szám 1-et eredményez:
KP = Kç (RT)0
KP = Kç x 1
KP = Kç
Az anyajegyek számának változását az alábbiakkal számolják:
∆n = A termékek molszáma - A reagensek molja
Ebben a számításban csak a gáz halmazállapotú anyagok együtthatói vesznek részt.
Minden alternatív egyenletre alkalmazva:
| acél-2g) + H2. g) ↔ COg) + H2Og) | ∆n = [(1 + 1) - (1 + 1)] = 2 - 2 = 0 |
| b) H2. g) + ½ a2. g) ↔ H2O(1) | ∆n = [0 - (1 + 1/2)] = 0 - 3/2 = - 3/2 |
| c) Nem2. g) + 3 H2. g) ↔ 2 NH3. g) | ∆n = [2 - (1 + 3)] = 2 - 4 = - 2 |
| d) NEMg) + ½ a2. g) ↔ NEM2. g) | ∆n = [1 - (1 + 1/2)] = 1 - 3/2 = - 1/2 |
| e) 4 FeSs + 7 O2. g) ↔ 2 Fe2O3 (s) + 4 SO2. g) | ∆n = [(0 + 4) - (0 + 7)] = 4 - 7 = - 3 |
Ezekkel az eredményekkel megfigyelhetjük, hogy az első egyenletben szereplő alternatíva, amelynek értéke megfelel a kívánt eredménynek.
6. (UEL-adaptált) A reakcióval, amelyet képvisel az egyensúlyi állandó Kç és KP egyenletekkel fejezzük ki: (Adva: p = parciális nyomás)
Helyes alternatíva:
Az egyensúlyi állandó kiszámítása:
A szilárd vegyületek állandó koncentrációik miatt nem vesznek részt a K számításábançezért az adott egyenlet egyensúlyi állandója:
Az egyensúlyi állandó szempontjából a nyomást tekintve csak a gázok vesznek részt a számításban, tehát:
Az egyensúlyi állandó kiszámítása
7. (Enem / 2015) Számos savat alkalmaznak olyan iparágakban, amelyek szennyvizeiket víztestekben, például folyókban és tavakban ártalmatlanítják, amelyek befolyásolhatják a környezeti egyensúlyt. A savasság semlegesítése érdekében a szennyvízbe megfelelő mennyiségben kalcium-karbonát-sót adhatunk, mivel hidrogén-karbonát keletkezik, amely semlegesíti a vizet. A folyamatban szereplő egyenletek bemutatásra kerülnek:
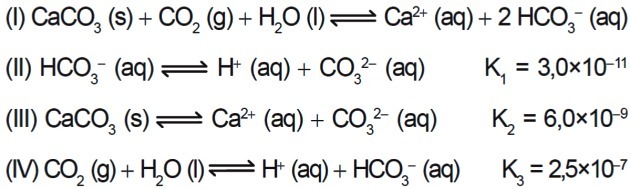
A II., III. És IV. Reakció 25 ° C-os egyensúlyi állandóinak értékei alapján mekkora az I. reakció egyensúlyi állandójának számértéke?
a) 4,5 x 10-26
b) 5,0 x 10-5
c) 0,8 x 10-9
d) 0,2 x 105
e) 2,2 x 1026
Helyes válasz: b) 5,0 x 10-5
1. lépés: Hess törvényének felhasználásával végezze el a szükséges kiigazításokat.
Adott kémiai egyenlet:
Az állandó kiszámítása:
De ha megfordítjuk az egyenletet, akkor ennek eredményét kapjuk:
És az állandó inverz lesz:
A kérdésben megadott 1. egyenlet eléréséhez meg kell fordítanunk a II. Egyenletet, az előző példához hasonlóan.
2. lépés: A II, III és IV egyenletek manipulálása az I. egyenlet eredményének eléréséhez
3. lépés: számítsa ki az I. egyenlet egyensúlyi állandóját
K kiszámításaén az állandó értékek szorzásával történik.
Mivel a számítás során egyenlő bázishatalommal rendelkezünk, megismételjük az alapot és hozzáadjuk a kitevőket.
Mivel most van egy egyenlő bázishatalommal rendelkező felosztás, megismételjük az alapot és kivonjuk a kitevőket.
8. (UnB) A foszfor-pentaklorid nagyon fontos reagens a szerves kémia területén. A reakció során gázfázisban állítják elő:
Egy 3,00 literes palack egyensúlyban, 200 ° C-on: 0,120 mol PCI-t tartalmaz5g)0,600 mol PCI3g) és 0,0120 mol CL2g). Mekkora az egyensúlyi állandó értéke ezen a hőmérsékleten?
Helyes válasz: 50 (mol / L)-1
1. lépés: Állítsa össze az egyensúlyi állandó kifejezését a reakcióhoz.
2. lépés: Számítsa ki az egyensúlyi komponensek koncentrációit mol / l-ben.
Moláris koncentráció képlete:
| PCl3 | Cl2 | PCl5 |
3. lépés: cserélje ki a konstans kifejezésben lévő koncentrációkat és számítsa ki a K értékétç.
Egyensúlyi egyensúlyi alkalmazások
9. (Enem / 2016) Teljes abroncsuk után az abroncsok elégethetők, hogy energiát termeljenek. A vulkanizált gumi teljes elégetésénél keletkező gázok közül néhány szennyező anyagot tartalmaz, és savas esőt okoz. Annak megakadályozása érdekében, hogy a légkörbe kerüljenek, ezeket a gázokat megfelelő anyagot tartalmazó vizes oldatba lehet buborékoltatni. Vegye figyelembe a táblázatban felsorolt anyaginformációkat.
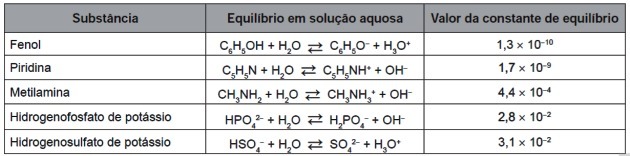
A táblázatban felsorolt anyagok közül az képes a leghatékonyabban eltávolítani a szennyező gázokat (a)
a) fenol.
b) Piridin.
c) metil-amin.
d) Kálium-hidrogén-foszfát.
e) Kálium-hidrogén-szulfát.
Helyes válasz: d) Kálium-hidrogén-foszfát.
a CO2, kén-oxidok (SO2 és aztán3) és nitrogén-oxidok (NO és NO2) a fő szennyező gázok.
Amikor a légkörben jelen lévő vízzel reagálnak, akkor a savképződés amelyek az eső savasságának növekedését okozzák, ezért nevezik savas esőnek.
A táblázatban megadott egyensúlyi állandókat a termékek és a reagensek koncentrációinak aránya alapján számoljuk ki az alábbiak szerint:
Vegye figyelembe, hogy az egyensúlyi állandó arányos a termékek koncentrációjával: minél nagyobb a termékmennyiség, annál nagyobb a K értékeç.
Jegyezze fel az első és az utolsó összetett értékeket a táblázatban a K értékreç:
| piridin | ||
| Kálium-hidrogén-szulfát |
A két számot összehasonlítva azt látjuk, hogy minél kisebb a negatív teljesítmény, annál nagyobb az állandó értéke.
A szennyező anyagok hatékonyabb eltávolítása érdekében OH- hogy reagáljon H-ionokkal+ savakban jelen van a semlegesítési reakció.
A bemutatott anyagok közül a savas vegyületek semlegesítéséhez szükséges hidroxilokat állítják elő: piridin, metil-amin és kálium-hidrogén-foszfát.
Annak kiderítésére, hogy melyik vegyület a leghatékonyabb, megfigyeljük az egyensúlyi állandókat: minél nagyobb az állandó érték, annál nagyobb az OH koncentrációja-.
Így az erre a célra alkalmas anyagot tartalmazó vizes oldat kálium-hidrogén-foszfát, mivel bázikusabb és hatékonyabban semlegesíti a savakat.
További információkért olvassa el ezeket a szövegeket.:
- ionmérleg
- Semlegesítési reakció
10. (Enem / 2009) A szappanok hosszú láncú karbonsavak sói, amelyeket a a mosási folyamatok során az alacsony vízoldékonyságú anyagok, pl. olajok és zsírok. A következő ábra a szappanmolekula szerkezetét mutatja.
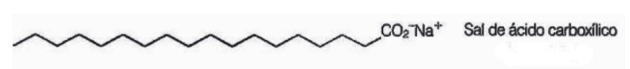
Oldatban a szappananionok hidrolizálhatják a vizet és ezáltal a megfelelő karbonsavat képezhetik. Például a nátrium-sztearát esetében a következő egyensúly alakul ki:
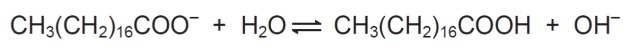
Mivel a képződött karbonsav rosszul oldódik vízben és kevésbé hatékony a zsírok eltávolításában, a táptalaj pH-ját úgy kell ellenőrizni, hogy megakadályozzuk a fenti egyensúly jobbra tolódását.
A szövegben szereplő információk alapján helyes azt a következtetést levonni, hogy a szappanok valamilyen módon működnek:
a) Bázikus pH-n hatékonyabb.
b) savas pH-nál hatékonyabb.
c) Hatékonyabb semleges pH-n.
d) Hatékony bármilyen pH-tartományban.
e) Hatékonyabb savas vagy semleges pH-n.
Válasz: a) Bázikus pH-n hatékonyabb.
A bemutatott egyensúlyban azt látjuk, hogy a nátrium-sztearát vízzel reagálva karbonsavat és hidroxilt képez.
A pH szabályozásának célja nem az, hogy lehetővé tegye a karbonsav képződését, és ez az egyensúly eltolásával történik az OH koncentrációjának megváltoztatásával.-.
annál inkább OH- az oldatban zavar van a termék oldalán, és a kémiai rendszer úgy reagál, hogy elfogyasztja az anyagot, amelynek koncentrációja megnőtt, ebben az esetben a hidroxilt.
Következésképpen a termékek reagensekké alakulnak.
Ezért a szappanok bázikus pH-n működnek a leghatékonyabban, mivel a hidroxilfelesleg balra tolja az egyensúlyt.
Ha a pH savas lenne, nagyobb lenne a H koncentrációja+ ami az OH fogyasztásával befolyásolná az egyensúlyt- és az egyensúly több hidroxil termelésével, az egyensúly balra tolásával és több karbonsav termelésével hatna, ami nem érdekes a bemutatott eljárás szempontjából.
Kémiai egyensúly eltolódása
11. (Enem / 2011) Az üdítők egyre inkább a közegészségügyi politikák célpontjává váltak. A ragasztószerek foszforsavat tartalmaznak, amely anyag káros a kalcium rögzítésére, az ásványi anyag, amely a fogmátrix fő alkotóeleme. A fogszuvasodás az egyensúlyhiány dinamikus folyamata a fogak demineralizációjában, az ásványi anyagok vesztesége a savasság miatt. Ismert, hogy a fogzománc fő összetevője egy hidroxiapatit nevű só. A szóda a szacharóz jelenléte miatt csökkenti a biofilm (bakteriális plakk) pH-ját, ami a fogzománc demineralizációját okozza. A nyálvédő mechanizmusok 20-30 percet vesznek igénybe a pH-szint normalizálásához, a fog remineralizálásához. A következő kémiai egyenlet képviseli ezt a folyamatot:
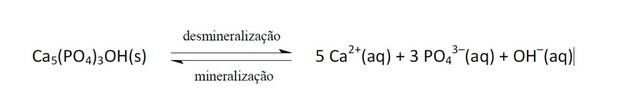 GROISMAN, S. A szódának a fogakra gyakorolt hatását felmérik anélkül, hogy levennék az étrendről. Elérhető: http://www.isaude.net. Hozzáférés ideje: 2010. május 1. (kiigazított szöveg).
GROISMAN, S. A szódának a fogakra gyakorolt hatását felmérik anélkül, hogy levennék az étrendről. Elérhető: http://www.isaude.net. Hozzáférés ideje: 2010. május 1. (kiigazított szöveg).
Figyelembe véve, hogy egy személy naponta fogyaszt üdítőitalokat, előfordulhat a fogak demineralizációjának folyamata a megnövekedett
a) OH–, amely reagál a Ca-ionokkal2+, jobbra tolva az egyensúlyt.
b) H+, amely reagál az OH hidroxilokkal–, jobbra tolva az egyensúlyt.
c) OH–, amely reagál a Ca-ionokkal2+, balanccsal eltolva az egyensúlyt.
d) H+, amely reagál az OH hidroxilokkal–, balanccsal eltolva az egyensúlyt.
e) Ca2+, amely reagál az OH hidroxilokkal–, balanccsal eltolva az egyensúlyt.
Helyes válasz: b) H+, amely reagál az OH hidroxilokkal–, jobbra tolva az egyensúlyt.
Amikor a pH csökken, azért van, mert megnőtt a savasság, vagyis a H-ionok koncentrációja+, amint a közlemény mondja, foszforsav van jelen.
Ezek az ionok reagálnak OH-val- ennek az anyagnak az elfogyasztása és következésképpen az egyensúly jobbra tolása, mivel a rendszer ezeknek az eltávolított ionoknak a további termelésével hat.
A reaktánsok és a termékek közötti egyensúlyeltolódás az OH koncentráció csökkenése miatt következett be-.
Ha a Ca-ionok2+ és ó- Ha a koncentráció nőtt, az egyensúlyt balra tolta, mivel a rendszer úgy reagált, hogy elfogyasztotta őket, és több hidroxi-apatitot képezett.
A hűtőközeg szivárgásával kapcsolatos korábbi mérleg megváltoztatása a leírt feltételek mellett a következőket eredményezi:
a) CO felszabadulás2 a környezet számára.
b) A tartály hőmérsékletének emelése.
c) A tartály belső nyomásának emelkedése.
d) A CO-koncentráció emelkedése2 a folyadékban.
e) Jelentős mennyiségű H képződése2O.
Helyes válasz: a) CO felszabadulás2 a környezet számára.
A palack belsejében a szén-dioxid feloldódott a folyadékban a nagy nyomás miatt.
Amikor az üveget kinyitják, a tartály belsejében lévő nyomás (amely nagyobb volt) megegyezik a környezet nyomásával, és ezzel a szén-dioxid kiszabadul.
A reaktánsok és a termékek közötti egyensúlyeltolódás a nyomás csökkenése miatt következett be: amikor a nyomás csökken, az egyensúly a legnagyobb térfogatra (molszámra) tolódik.
A reakció balra tolódott és a CO2 amely feloldódott a folyadékban, felszabadult, és az üveg kinyitásakor kiszivárgott.