A pályák Linus Pauling által 1960-ban létrehozott modellje szerint a kovalens kötés, amely a A molekulák a molekulában részt vevő elemek hiányos pályáinak fúziójával vagy behatolásával következnek be Link. Így arra a következtetésre jutottak, hogy ha az elemnek hiányos a pályája (csak egy elektronnal rendelkezik), akkor csak kovalens kötést hozhat létre. Ha két hiányos pályája van, akkor legfeljebb két kapcsolatot tud létrehozni stb.
Nézze meg azonban a szénatom elem atompályáit, amelynek atomszáma 6 (Z = 6):
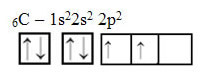
Ne feledje, hogy két hiányos pályája van, ezért legfeljebb két kötést kell végrehajtania. Vele azonban nem ez történik. Mint sokan tudják, a szén négy kötést hoz létre (négyértékű), ezért a pályák ezen modellje nem magyarázza meg a szén esetét.
Ennek a zsákutcának a végére egy új elméletet hoztak létre, amely jobban megmagyarázta ezt a kérdést: a Hibridizációs elmélet.

Ez azt jelenti, hogy a hibridizáció a tiszta pályák „keveréke”.
A szén esetében a hibridizációnak három típusa van: sp3, sp2 és sp.
A hibridizáció létrejöttének megértéséhez nézzük meg a szénhibridizáció első típusát, az sp típust.3:
Ez a fajta hibridizáció a metánmolekulában (CH4). Megjegyezzük, hogy négy központi kovalens kötés van a szén, amely a központi elem, és négy hidrogén között. Tehát nézze meg, mi a hiányos hidrogén pálya:
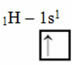
Mivel mindegyik hidrogén hiányos s-típusú pályával rendelkezik, szükség van még egy elektron befogadására, vagyis mindegyik csak egy kovalens kötést köt a szénnel. Ezért a szénnek négy hiányos pályájával kell rendelkeznie. Hogyan történik ez? Hibridizáció útján.
Amikor a 2s pályáról egy elektron elnyeli az energiát, az az üres 2p pályára kerül. Így azt mondjuk, hogy az elektron ezen ugrása a 2-esektől a 2p-es alszintig az elektron „előmozdítása”. Ily módon a szén gerjesztett vagy aktivált állapotban marad, négy hibridizált orbitális áll rendelkezésre a kovalens kötések végrehajtására:
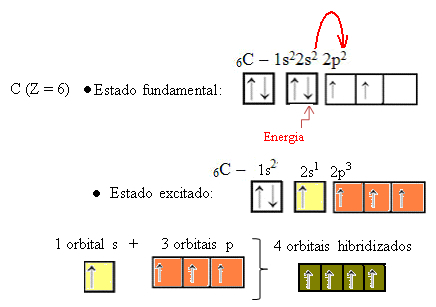
Vegye figyelembe, hogy a kialakult hibrid pályák egyenértékűek egymással, de különböznek az eredeti tiszta pályáktól.
Ily módon a négy hidrogénatom s-pályája közötti kötés ezen négy hibridizált szénpályával fordul elő:
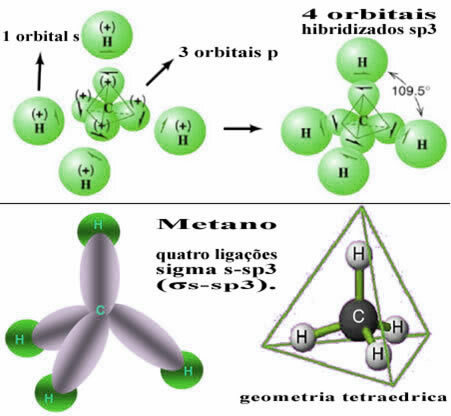
Mint fent látható, a metánmolekula szabályos tetraéderszerkezettel rendelkezik, minden csúcsban a négy elektronfelhő és a szomszédos szögek 109 ° 28 ’. Mivel a kötés minden hidrogén s pályája és egy hibridizált sp orbitális között létrejött3 minden kapcsolatnál akkor megvan, hogy vannak négy sigma s-sp link3 (σs-sp3).
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp3.htm