Az érzékeny hő vagy az érzékeny fajlagos hő olyan fizikai mennyiség, amely a test hőmérsékletének változásával függ össze.
Példa: Fémrúd fűtése
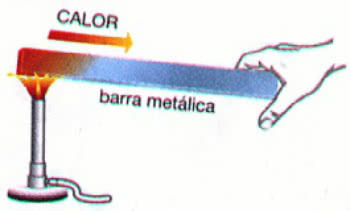
A fenti példában a hő a hővezetés. Ez a folyamat az anyag hőmérsékletének emelkedését eredményezi, azonban fizikai állapota változatlan (szilárd).
Képlet
Az érzékeny hő kiszámításához a következő képletet kell használni:
Q = m. ç. Δθ
Q: érzékeny hőmennyiség (mész vagy J)
m: testtömeg (g vagy kg)
ç: az anyag fajlagos hője (cal / g ° C vagy J / Kg ° C)
Δθ: hőmérséklet-változás (° C vagy K)
jegyzet: Az érzékeny hő kiszámításához ismerni kell az egyes anyagokban változó fajlagos hőt.
További információ: Fajlagos hő.
Érzékeny hő és látens hő
A látens hő (L), az anyag fizikai állapota módosul, míg érzékeny melegben ugyanaz marad.
A másik különbség a hőmérséklet között van. Vagyis a látens hő független a test hőmérsékletétől, míg az érzékeny hő ezt figyelembe veszi.
A látens hőre példa a jégkocka megolvadása vagy a víz elpárologtatása. Mindkét esetben a hőmérséklet a két fizikai állapotban ugyanaz marad.
A látens hő kiszámításához használja a következő képletet:
Q = m. L
Hol,
Q: hőmennyiség (mész vagy J)
m: tömeg (g vagy kg)
L: látens hő (cal / g vagy J / kg)
Olvassa el:
- Hő és hőmérséklet
- Kalorimetria
- Hőmérleg
- Hőkapacitás
- Fizika képletek
Felvételi vizsga gyakorlatok visszajelzéssel
1. (Mackenzie) A hőforrás folyamatosan, 150 cal / s sebességgel táplálja a hőt egy adott víztömeghez. Ha a víz hőmérséklete 4 perc alatt 20 ° C-ról 60 ° C-ra emelkedik, és a víz fajhő-érzékeny értéke 1,0 cal / g ° C, akkor arra lehet következtetni, hogy a felmelegített víz tömege grammban:
a) 500
b) 600
c) 700
d) 800
e) 900
Alternatív és
2. (UFSM-RS) 400 g testet és 0,20 cal / g ° C érzékeny fajlagos hőt 10 ° C hőmérsékleten helyezünk el. termikus érintkezésben további 200 g testtel, és érzékeny fajlagos hővel, 0,10 cal / g ° C, 20 ° C hőmérsékleten 60 ° C. A két test közötti hőegyensúly létrejötte után a végső hőmérséklet a következő lesz:
a) 14 ° C
b) 15 ° C
c) 20 ° C
d) 30 ° C
e) 40 ° C
Alternatív c
3. (UFPR) A napfogyatkozás során a totalitás zóna egyik városában, Criciúma - SC-ben 8,0 ° C-os hőmérséklet-csökkenés volt tapasztalható. (Nulla óra - 1994.04.11.)
Annak tudatában, hogy a víz érzékeny fajhője 1,0 cal / g ° C, az 1000 g víz által kibocsátott hőmennyiség, ha a hőmérsékletét mészben 8,0 ° C-ról csökkentik:
a) 8.0
b) 125
c) 4000
d) 8000
e) 64000
Alternatív


