úgy definiálja magát hibridizáció a hiányos atompályák egyesülése. Egy pálya hiányosnak minősül, ha csak egy van elektron benne kettő helyett. Lásd a hiányos pálya és a teljes pálya ábrázolását:

Az A képen egy teljes pálya van; a B képen hiányos pálya.
A hibridizáció olyan természetes jelenség, amely bizonyos kémiai elemekkel fordul elő, például foszfor, kén, szén stb. A szén hibridizációja lehetővé teszi, hogy ennek az elemnek az atomjai képesek legyenek négy kémiai kötést létrehozni, vagyis a szén csak négy kötést hoz létre, miután átesik a hibridizáció jelenségén.
De miért hibridizálódik a szén és köt négy kötést? A jelenség megértéséhez ismerni kell ennek az elemnek az elektronikus terjesztését:
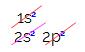
A szén elektronikus eloszlásában azt látjuk, hogy az 1s alszint teljes (két elektronnal), a 2s teljes (két elektronnal), és a 2p alszint hiányos (a p alszint hat elektront támogat, de csak kettő). A 2p elektronokat reprezentatív módon elosztva:
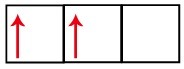
A p alszintnek három pályája van - a szén esetében kettő hiányos, egy pedig üres. Ezért ennek az elemnek csak két kapcsolatot kell végrehajtania, mivel a hiányos pályák száma mindig meghatározza a linkek számát.
Amikor azonban a külső környezetből energiát kapunk, a szénben jelen lévő elektronok izgatottak. Így a 2. alszint egyik elektronja átmegy a p alszint üres pályájára:
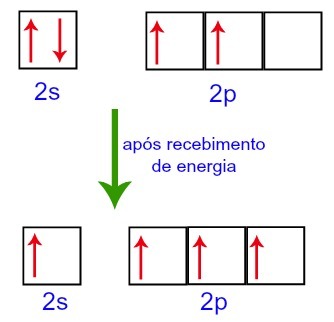
Szénpályák a külső környezetből származó energia befogadása előtt és után
Így a szénnek a második szintjén négy hiányos pályája marad. Ezután a 2s alszint pályája összekapcsolja a három p pályát, ami konfigurálja a jelenséget hibridizáció.
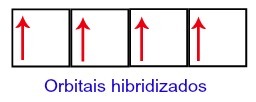
Szénpályák hibridizáció után
Általam. Diogo Lopes Dias
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/hibridizacao-carbono.htm
