Ön oxidok két különböző elemből állnak, az egyik oxigén, amelynek a kettő közül a legelegatívabbnak kell lennie.
A szervetlen oxidok nómenklatúrája olyan szabályokat követ, amelyek attól függenek, hogy az oxid molekuláris, kovalens vagy ionos-e. Nézzük meg az egyes eseteket:
* Molekuláris oxidok vagy kovalens hálózat nomenklatúrája:
Molekuláris vagy kovalens hálózati oxidok azok, amelyek oxigénjét a ametalpéldául szén (C), nitrogén (N), kén (S), fluor (F). Ezen oxidok nómenklatúrája a következő szabályt követi:

Nomenklatúra szabály az ametálokkal képződött oxidokra
Az oxigénnel kapcsolt elem előtt a mono előtag választható.
Például a következő molekuláris oxiddal rendelkezünk: CO.
- Az oxigén mennyiségét jelző előtag: 1 oxigén: monó;
- oxidja;
- Előtag, amely jelzi a másik elem atomszámát: 1 szén: monó;
- Az oxigénhez kapcsolódó elem neve: szén.
Tehát a neved így szól: CO = monokarbon monoxid vagy szén-monoxid.
További példák:
szén-dioxid - CO2
Kén-trioxid - SO3
Diklór-heptoxid - Cl2O7
Dinitrogén-monoxid - N
Dinitrogén-trioxid - N2O3
Nitrogén-monoxid -NO
Nitrogén-dioxid - NEM2
Dinitrogén-pentoxid - N2O5
Szilícium-dioxid - SiO2
Difoszfor-pentoxid - P2O5
Kén-trioxid - SO3
* Az ionos oxidok nomenklatúrája:
Az ionos oxidok azok, amelyek oxigénhez kötődnek a fémmint például vas (Fe), ólom (Pb), nátrium (Na), kalcium (Ca), ezüst (Ag). Általában az oxigén elektromos töltése -2.
A molekuláris vagy kovalens hálózati oxidokra említett nómenklatúrát jelenleg a fémoxidokra is alkalmazzák, és hivatalosnak tekintik. Néhány példa:
Vas-monoxid - FeO
Ólom-monoxid - PbO
Ólom-dioxid - PbO2
Különböző trioxid - Fe2O3
Van azonban egy speciális nómenklatúra a fém-oxidok számára, amelyet még mindig széles körben használnak. Az oxigénhez kapcsolódó elem vegyértékén alapul.
Ha az elem rendelkezik egyetlen vegyérték, azaz ha csak egy módon lehet megkötni az oxigént és csak egy típusú oxidot képezni, akkor a névadási szabályt a következők adják meg:

Egy vegyértékű ionos oxid elnevezési szabály
Példák:
- Nátrium-oxid - Na2O
- Kalcium-oxid - CaO
- Kálium-oxid - K2O
- Alumínium-oxid - Al2O3
- Ezüst-oxid - Ag2O
De vannak olyan ionos oxidok is, amelyeket a több mint egy vegyérték. Ezekben az esetekben a névadási szabály a következő:
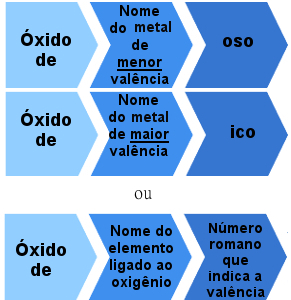
Nómenklatúra szabály több vegyértékű ionos oxidokra
Példák:
Vas-oxid - FeO
Vas-oxid - Fe2O3
Réz-oxid - Cu2O
réz-oxid - CuO
Vagy:
Vas-oxid II - FeO (Vas-nox = +2)
Vas-oxid III - Fe2O3 (Vasszám = +3).
Réz-oxid I - Cu2O (vasszám = +1)
Réz-oxid II - CuO (vashox = +2).
Írta: Jennifer Fogaça
Kémia szakon végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-oxidos.htm

