A sűrűség egy fizikai mennyiség, amely a a test anyagának koncentrációja egy adott térfogatban.
Ezt a testtömeg és a térfogat arányával kapják meg, és kg / m-ben mérik3 az egységek nemzetközi rendszerében (SI).
A test sűrűsége fordítottan arányos a térfogatával, vagyis minél nagyobb a térfogata, annál kisebb a sűrűsége. Vegye figyelembe ezt a kapcsolatot a sűrűség képletében:

A sűrűség az a tulajdonság, amely meghatározza, hogy egy test lebeg-e vagy süllyed egy folyadékban. Ha az anyag kevésbé sűrű, mint a folyadék, akkor lebeg, de ha a sűrűsége nagyobb, mint a folyadéké, süllyed.
A természetben található összes anyag mérhető sűrűségű. A sűrűség a anyagtípus, nak,-nek fizikai állapot hol találja magát és annak feltételei hőfok és környezeti nyomás.
Hogyan lehet kiszámítani a sűrűséget?
Egy anyag vagy anyagkeverék sűrűségének kiszámításához ossza el a test tömegét térfogatával a következő képlet szerint:
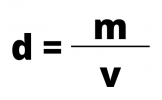
Hol:
- d = sűrűség kg / m-ben mérve3, g / cm3 vagy g / ml
- m = tömeg kg-ban vagy g-ban mérve
- v = m-ben mért térfogat3, cm3 vagy ml
Fontos szem előtt tartani, hogy mivel a test térfogata változik a hőmérséklet és a nyomás különböző körülményei között, a hőmérséklet és a nyomás változásakor a sűrűség más és más lesz.
Például a víz sűrűsége körülbelül 1 g / cm3 környezeti állapotban, de amikor jéggé válik, a sűrűsége 0,92 g / cm-re csökken3 - ez a sűrűségbeli különbség miatt úszik a vízen a jég.
 A jég a vízen úszik, mert szilárd állapotban kisebb a sűrűsége, mint folyékony állapotban.
A jég a vízen úszik, mert szilárd állapotban kisebb a sűrűsége, mint folyékony állapotban.
Gyakorlati példák a sűrűségre
Ahhoz, hogy a gyakorlatban megértsük, mi a sűrűség, képzeljen el két edényt, az egyikben 1 kg ólom, a másikban 1 kg pamut. Mindkettő tömege azonos, azaz 1 kg.
Mivel azonban a gyapot sokkal könnyebb, mint az ólom, ennél az anyagnál sokkal nagyobb mennyiségre van szükség mindkét tartály tömegének kiegyenlítéséhez.
Így a pamut által elfoglalt tér sokkal nagyobb lesz, mint az ólom által elfoglalt tér. Ez azt jelenti, hogy az ólomnak sokkal nagyobb a koncentrált anyagmennyisége, ezért nagyobb a sűrűsége, mint a gyapotnak.
Most nézzen meg más példákat a gyakorlati helyzetekre, amelyeket az anyagok sűrűségének különbsége magyaráz:
Jégkockák
Egy pohár vízbe helyezve a jégkockák lebegnek, mert sűrűségük (0,92 g / cm)3) kisebb, mint a víz sűrűsége (1g / cm3).
Ha jégkockákat helyezünk egy pohár alkoholba, a jégkockák elsüllyednek, mert sűrűségük (0,92 g / cm)3) nagyobb, mint az etanol sűrűsége (0,79 g / cm3).
 A jég egy pohár alkoholos italba süllyed, mert az alkohol sűrűsége kisebb, mint a vízé.
A jég egy pohár alkoholos italba süllyed, mert az alkohol sűrűsége kisebb, mint a vízé.
Hungarocell és köröm
Egy másik példa, amely segít megérteni a sűrűséget, megfigyelni a hungarocell tábla és az acélból készült szegek viselkedését vízbe helyezve.
A köröm azonnal elsüllyed, mert sűrűsége (0,78 g / m)3) sokkal nagyobb, mint a víz sűrűsége. Ez azt jelenti, hogy az acél nagy mennyiségű anyagot tartalmaz kis térfogatban.
Másrészt, ha a hungarocelltáblát vízbe helyezik, az lebeg, mivel a hungarocell sűrűsége kisebb, mint a víz sűrűsége. Az acéltól eltérően a hungarocell olyan anyag, amely kevés koncentrált anyagot tartalmaz.
 A hungarocell sűrűsége kisebb, mint a vízé, ezért a deszka lebeg.
A hungarocell sűrűsége kisebb, mint a vízé, ezért a deszka lebeg.
Fajlagos tömeg és sűrűség
A sűrűséget a sűrűségre is utalják, de ezeket nem mindig lehet szinonimaként értelmezni.
A sűrűség utal a test, amely csak egy anyagból vagy anyagok keverékéből állhat, például víz és cukor oldata.
A Különleges tömegviszont utal az a sűrűségére homogén anyag specifikus, például alumínium, ólom vagy víz.
Ez azt jelenti, hogy amikor a test csak egy anyagból áll, sűrűségét a fajlagos tömege adja. Ha azonban a test heterogén, akkor a sűrűségét a tömeg és a térfogat arányában kell kiszámítani.
Anyagsűrűség
Néhány anyag sűrűségét (vagy fajsúlyát) lásd az alábbi táblázatban:
| Anyag | Sűrűség |
|---|---|
| Víz | 1,0 |
| Levegő | 1,2 |
| Acél | 7,8 |
| Alumínium | 2,7 |
| Vezet | 11,3 |
| Réz | 8,9 |
| Etanol | 0,79 |
| Vas | 7,86 |
| Jég | 0,92 |
| Tej | 1,03 |
| faipari | 0,5 |
| Arany | 19,3 |
Abszolút sűrűség és relatív sűrűség
Az abszolút sűrűség egy adott test vagy anyag sűrűségére utal. A relatív sűrűség viszont az egyik anyag sűrűsége a másikhoz képest.
A relatív sűrűség kiszámítása a két sűrűség aránya, amelyet úgy számolunk, hogy a tömeget elosztjuk a térfogattal. A sűrűség képlet az alábbiakkal fejezhető ki:
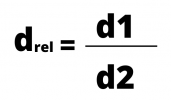
vagy
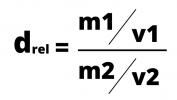
A relatív sűrűséget gyakran használják az anyagok sűrűségének összehasonlításához a vízhez viszonyítva, amelynek sűrűsége 1g / cm3.
Sűrűség mértékegysége
A nemzetközi rendszerben (SI) alkalmazott mértékegysége kg / m3, de gyakori, hogy ezt a nagyságrendet g / cm-ben is kifejezzük3 és g / ml. Ezen mértékegységek közötti kapcsolat a következő:
1 g / cm3 = 1 g / ml = 1000 kg / m3
Lásd még: kémia és térfogatmérések.

