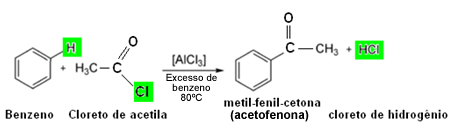
Nál nél kovalens kötések, más néven molekuláris vagy homopoláris kötések, azok, amelyek az atomok között fordulnak elő elektronegatív elemek, azaz hajlamos az elektronok befogadására, megkötve a elektronok megosztása vegyértékhéjaikból.
A következő elemek között kovalens kötés fordulhat elő: hidrogén, nemfémek és félfémek. A fémek soha nem vesznek részt ilyen típusú kötésben.
Vizsgáljuk meg a kovalens kötés egyszerű példáját: a hidrogéngázt képző kötést (H2):
H + H → H2
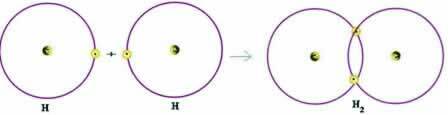
Megjegyezzük, hogy mindkét atomnak elektront kellett kapnia a vegyértékhéj teljesítéséhez - az Octet-szabály szerint - és ily módon stabilnak kell maradnia. Ezért megosztották egymással az elektronjaikat, és ily módon mindkettőjüknek két elektronja volt, teljes K-héjuk volt, és megszerezték a nemesgáz-hélium konfigurációját.
Ez az elektronmegosztás különbözteti meg ezt a kötéstípust az ionos kötéstől, amelyben az elektrontranszfer zajlik.
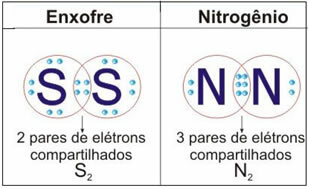
További két példát az esetre az alábbi ábrán talál:
Ne álljon meg most... A reklám után még több van;)
Az ilyen típusú kötésekben molekulák képződnek, amelyeket a megfelelőik képviselhetnek molekuláris képletek, vagyis a legegyszerűbb ábrázolás, amely azt jelzi, hogy az egyes elemek hány atomja van a molekulában. Néhány példa a molekulaképletekre: H2, S2, O2, nem2, H2O, CO2stb.
A kovalens kötést két másik képlettel ábrázolhatjuk:
- Elektronikus képlet vagy Lewis képlet: ebben a képletben megjelennek az egyes atomok vegyértékhéjának elektronjai és az elektronikus párok kialakulása is. Ezeket az elektronokat a jelek szimbolizálják . vagy x;
- Lapos szerkezeti képlet vagy Couper szerkezeti képlet: az elemek linkjeit mutatja, minden megosztott párnak kötőjelnek felel meg. Ha ez csak egy kötőjel, akkor egyetlen linknek hívjuk; ha kettő van, kettős kötés; és ha három kötőjel van, hármas kötés.
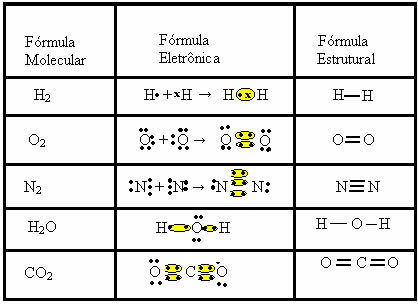
Vegye figyelembe a kovalens kötések más példáit, amelyeket ez a három kémiai képlet képvisel:
Írta: Jennifer Fogaça
Kémia szakon végzett
Hivatkozni szeretne erre a szövegre egy iskolai vagy tudományos munkában? Néz:
FOGAÇA, Jennifer Rocha Vargas. "Kovalens kötések"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/ligacoes-covalentes.htm. Hozzáférés: 2021. június 27.