O hő és a Hőenergia, a különbség motiválta hőfok, amely a magasabb hőmérsékletű testből az alacsonyabb hőmérsékletű testbe áramlik. Az energiaáramlás a különböző hőmérsékletű testek között addig tart, amíg el nem éri a hőmérleg, amikor a hőcserélő testek hőmérséklete egyenlővé válik.

Még akkor is, ha a Nemzetközi mértékegység-rendszer (SI) határozza meg, hogy az energia mértékegysége joule (J), a hőhöz leggyakrabban használt egység a kalória (cal). Egy kalória megfelel annak a hőmennyiségnek, amely ahhoz szükséges, hogy 1 g víz hőmérséklet-ingadozása 14,5 ° C és 15,5 ° C között legyen.
A kalória és a joule közötti megfelelés az, hogy 1 cal körülbelül 4,18 J.
érzékelhető hő
Amikor egy test megkap vagy ad egy bizonyosat hőmennyiség, csak hőmérsékleti ingadozásokat képes létrehozni, anélkül, hogy bekövetkezne a molekulák aggregációs állapotának változása, a meleget nevezzük érzékeny.
A következő egyenlet segítségével meghatározható a test által kapott vagy elveszített érzékeny hő mennyisége.
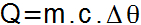
Ebben az egyenletben a megfelelő elemek és mértékegységek a következők:
Q = Érzékeny hő mennyisége (mész);
m = Anyag tömege (g);
c =fajlagos hő (cal / g ° C);
Δθ = Hőmérséklet-változás (° C vagy K).
Két megfigyelés fontos:
O fajlagos hő az egyes anyagtípusok jellemző mennyisége, amely meghatározza az 1 g elem hőmérsékletének 1 ° C-os emeléséhez szükséges hőmennyiséget.
A hőmérséklet-változások mindkettőben kifejezhetők ° C mennyi be K, mert ez a kettő Mérleg van 100 intervallum, ezzel bemutatva a ugyanazok a variációk.
Példa
Határozza meg az érzékeny hő mennyiségét, amely szükséges egy adott anyag 4 kg-os mintájának 40 ° C és 50 ° C közötti hőmérséklete, amelynek fajlagos hője 0,5 cal / g ° C.
Kérdés adatai:
M tömeg: m = 4 kg = 4000 g
Hőmérsékleti tartomány: Δθ = 50 - 40 = 10 ° C
Fajlagos hő: c = 0,5 cal / g ° C
Q = m.c.Δθ
Q = 4000. 0,5. 10
Q = 20 000 cal = 20 kcal
Ez az anyagmennyiség 10 ° C-kal változik, ha 20 000 mész hőt kap.
Írta: Joab Silas
Fizikából végzett
Forrás: Brazil iskola - https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-calor-sensivel.htm

