A aktiválási energia ez a minimális energiamennyiség, amely a reagáló részecskék közötti, kedvező helyzetben történő ütközéshez szükséges és reakciót eredményez.
A reakciók csak akkor fordulnak elő, ha a reagensek aktiválási energiával rendelkeznek (vagy a minimálisan szükséges energiával, amely reakciótól függően változik; akár mennyiségben, akár formában), vagy amikor nekik szállítják.
Például, amikor a fém-nátrium vízzel érintkezik, hevesen reagál. Ez azt jelenti, hogy ezen reagensek energiatartalma már elegendő a reakció lejátszódásához.
A kályha bekapcsolása esetén az égési reakció csak akkor következik be, ha meggyújtott gyufát vagy más tűzforrást helyezünk a kályha által felszabaduló gáz közelébe. Ez azt jelenti, hogy ebben az esetben energiát kellett szállítani a rendszerbe, hogy elérje az aktivációs energiát és a reakció megtörténjen.
Magának a foszfornak az égésére az aktiválási energiát súrlódás biztosítja. Ugyanez történik az öngyújtókkal is, amelyeknek szintén szükségük van egy szikrára, amely megadja a szükséges aktiválási energiát a bennük lévő gáz elégetéséhez.
Az aktiválási energiát fény is biztosíthatja, mint például a hidrogén-peroxid bomlása esetén. Ezért tárolják sötét vagy átlátszatlan palackokban.
Ne álljon meg most... A reklám után még több van;)

Így arra a következtetésre juthatunk, hogy az aktivációs energia (Eamíg) a reakció elindulásához szükséges energia (E) és a reagensekben lévő energia (E.) különbségepr):

Az aktiválási energia akadályozza a reakció lejátszódását, és a reaktánsok kötéseinek megszakításához szükséges. Ezzel megtörténik a reakció, és új kapcsolatok jönnek létre a termékek kialakításához.
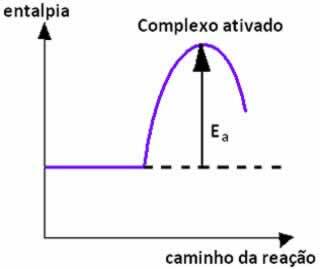
Amikor a kedvező orientációjú reagensek részecskéinek ütközése azonos energiával vagy magasabb, mint az aktivációs energia, a termékek képződése előtt egy köztes és instabil állapot alakul ki, denominált komplex aktiválva, amelyben a reaktáns kötések meggyengülnek és a termékkötések kialakulnak. Így, aktivációs energia az aktivált komplex kialakításához szükséges energia.
Az alábbiakban van egy grafikon, amely az aktiválási energiát mutatja a reakció lezárásának akadályaként:
Írta: Jennifer Fogaça
Kémia szakon végzett
Hivatkozni szeretne erre a szövegre egy iskolai vagy tudományos munkában? Néz:
FOGAÇA, Jennifer Rocha Vargas. "Aktiválási energia"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/energia-ativacao.htm. Hozzáférés: 2021. június 27.