ionizálás az a kémiai jelenség, amelyben egy savas anyag (amelynek általános képlete HX) vízben oldva két iont eredményez: hidronium-kationt (H3O+ vagy H+) és bármely anion (X-). A jelenséget egy egyenlet képviseli. Néz:
HX + H2O → H3O+ + X-
Az ionizáció során csak a sav hidronium-kationokká alakulnak át, amely tényező függ ennek a savnak az ionizációs képességétől, vagyis az ionizáció mértékétől (α) is. Így nem minden hidrogén képez hidroniumot, hacsak a sav ionizációs foka nem egyenlő 100% -kal.
Amikor azonban vagyunk ionizációs egyenlet felépítése, nem a sav ionizációjának mértékét vesszük figyelembe, hanem a mennyiségét ionizálható hidrogéneket hogy bemutatja.
Általános szabály, hogy az ionizálható hidrogént a hidrogén-savban lévő hidrogénnek tekintjük. Az oxisavak esetében csak a szénatomokhoz kötött hidrogének ionizálhatók, amint az az alábbiakban bemutatott szerkezeti képletről is kiderül:
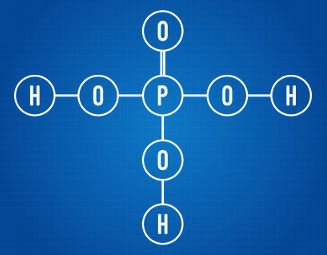
A foszforsavnak három ionizálható hidrogénje van
A fenti szerkezeti képletet elemezve láthatjuk, hogy a kérdéses savnak három hidrogénatomja kapcsolódik az oxigénatomokhoz. Mint ilyen, összesen három ionizálható hidrogénnel rendelkezik.
Lásd néhány szerelési példát egyes savak ionizációs egyenlete:
1. példa: Bróm-hidrogén-sav (HBr)
HBr + H2O → H3O+ + Br-
A hidrogén-bromid-sav olyan hidrogénsav, amelynek összetételében csak egy hidrogén van. Mivel a hidrogénsavban lévő összes hidrogén ionizálható, csak vízben oldódva képződik egy mol hidronium-kation ez a bromid-anion (Br-).
2. példa: Kénhidrogén (H2S)
H2Y + 2 H2O → 2 H+ + S-2
A hidrogén-szulfid egy hidrogén, amelynek összetételében két hidrogén van. Mivel a hidrogénsavban lévő összes hidrogén ionizálható, vízben oldódva képződik, két mol hidronium-kation ez a szulfidanion (S-2). Ehhez használtuk két mol vizet.
Ne álljon meg most... A reklám után még több van;)
3. példa: mangánsav (H2MnO4)
H2MnO4 + 2 H2O → 2 H3O+ + MnO4-2
A mangánsav egy oxisav, amelynek összetételében két hidrogén van. Mivel az oxisavakban csak az oxigénhez kötött hidrogén ionizálható - a mangánsav esetében a két hidrogén van -, vízben oldódva képződik, két mol hidronium-kation ez a manganát anion (MnO4-2). Ehhez használtuk két mol vizet.
4. példa: Foszforsav (H3POR3)
H3POR3 + 2 H2O → 2 H3O+ + HPO3-2
A foszforsav oxinsav, amelynek összetételében három hidrogén van. Mivel az oxisavakban csak az oxigénhez kötött hidrogén ionizálható - foszforsav esetében a két hidrogén -, vízben oldódva képződik, két mol hidronium-kation ez a foszfit anion (HPO3-2). Ehhez használtuk két mol vizet.
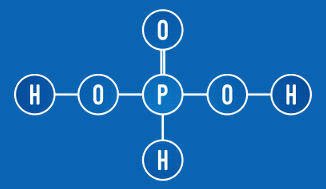
A foszforsavnak két ionizálható hidrogénje van (OH csoport)
5. példa: Bórsav (H3BO3)
H3BO3 + 3 H2O → 3 H+ + BO3-3
A bórsav oxi-sav, összetételében három hidrogén található. Mivel az oxisavakban csak az oxigénhez kötött hidrogén ionizálható - a bórsav esetében a három hidrogén van -, vízben oldva képződik, három mol hidronium-kation ez a borát anion (BO3-3). Ehhez használtuk három mol vizet.
6. példa: Pirofoszforsav (H4P2O7)
H4P2O7 + 4 H2O → 4 H3O+ + P2O7-4
A pirofoszforsav egy oxisav, amelynek összetételében négy hidrogén van. Mivel az oxisavakban csak az oxigénhez kötött hidrogén ionizálható - a bórsav esetében a négy hidrogén van -, vízben oldva képződik, négy mol hidronium-kation ez a anionpirofoszfát (P2O7-4). Ehhez használtuk négy mol vizet.
Általam. Diogo Lopes Dias
Hivatkozni szeretne erre a szövegre egy iskolai vagy tudományos munkában? Néz:
NAPOK, Diogo Lopes. "Savionizációs egyenletek"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/equacoes-ionizacao-dos-acidos.htm. Hozzáférés: 2021. június 28.