Ön aldehidek és a ketonok nagyon hasonló szerves funkciók. Mindkettőjük szerkezetében karbonilcsoport (C = O) van, azzal az egyetlen különbséggel, amely a aldehidek, mindig a szénlánc végén jelenik meg, vagyis az egyik karbonil-szén-ligandum a hidrogén; a ketonok karbonilja két másik szénatom között van.
Aldehid funkcionális csoport:A ketonok funkcionális csoportja:
O O
║ ║
C C ─ H C C ─ C
Emiatt vannak funkcionális izomerizmusok az aldehidek és a ketonok között. Például az alábbiakban két funkcionális izomert mutatunk be, amelyek molekuláris képlete megegyezik (C3H6O), de az egyik egy aldehid (propanal), a másik pedig egy keton (propanon). Nézze meg, hogyan változik ez teljesen a tulajdonságaikban és az alkalmazásokban:
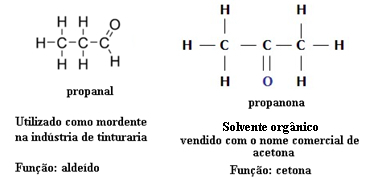
Példa az aldehid és a keton közötti funkcionális izomerizmusra
Képzelje el, hogy laboratóriumban van, és talál egy olyan színtelen folyadékot tartalmazó injekciós üveget, amelynek csak a C molekulaképlete van3H6O. Mit tennél, ha kiderítenéd, hogy ez keton vagy aldehid?
Az ilyen problémák megoldásához
vannak módszerek az aldehidek és ketonok megkülönböztetésére, ezeknek a vegyületeknek a gyenge oxidálószerekkel való reakcióján alapulva. Az alábbiak szerint gyenge oxidálószerekkel szembesülve az aldehidek oxidációval reagálnak, míg a ketonok nem. Ezt mondjukaz aldehidek redukálószerként működnek, de a ketonok nem, csak redukálószerként reagálnak energetikai oxidánsokkal érintkezve.Aldehidek + Gyenge oxidálószerek → karbonsav
O O
║ ║
C - C - H + [O] → C - C - OH
Ketonok + gyenge oxidálószerek → Ne reagáljon
O
║
C ─ C ─ C + [O] → Nincs reakció
Ennek alapján elegendő elvégezni ezt a reakciót, és megnézni, hogy a vegyület reagál-e vagy sem. Ha reagál, tudjuk, hogy ez aldehid; ha nem reagál, akkor keton.
Ezenkívül az ezekben az aldehid-oxidációs reakciókban képződött termékek jól láthatók, színváltozások következnek be, amint azt később bemutatjuk.
Az aldehidek és ketonok megkülönböztetésére három fő módszer létezik:
1- Tollens reaktív: Ez a reagens a ezüst-nitrát ammóniaoldata, azaz ezüst-nitrátot tartalmaz (AgNO3) és az ammónium-hidroxid feleslege (NH4OH):
AgNO3 + 3 NH4OH → Ag (NH3) OH + NH4A3 + 2 H2O
Tollens Reactive (nevét Bernhard Tollens (1841-1918) német vegyészről kapta)
Amint azt a szövegben kifejtettük Ezüsttükör készítéseHa egy aldehid reakcióba lép a Tollens-szel, oxidálódik a megfelelő karbonsavvá, míg az ezüstionok Ag-ra redukálódnak0 (fém ezüst). Ha ezt a reakciót például egy kémcsőben hajtják végre, akkor ez a fém ezüst lerakódik a cső falain, ami egy ezüst tükör. Ez a megfigyelt eredmény nagyon szép, és az ipari tükör gyártási folyamatában használják.
Ne álljon meg most... A reklám után még több van;)
A lejátszódó reakció a következőképpen ábrázolható:
O O
║ ║
R - C - H + H2O → R ─ C ─ OH + 2e- + 2 H+
2 Ag+ + 2e- → 2 Ag0
2 NH3 + 2 H+ → 2 NH4+
O O
║║
R C ─ H + 2 Ag+ + 2 NH3 + H2O → R C ─ OH + 2 Ag0 + 2 NH4+
aldehid Tollenek reaktívakkarbonsav fém ezüst (ezüst tükör)
Másrészt, ha a ketont reagáljuk a Tollens reaktív anyaggal, a fém ezüst képződése nem következik be, mivel a ketonok nem képesek csökkenteni az Ag ionokat.+.
2- Fehling reaktív: Ez a reaktív a réz-szulfát II kék oldata (CuSO4) bázikus közegben, miközben összekeverjük egy másik nátrium-hidroxid (NaOH) és nátrium- és kálium-tartarát (NaOOC-CHOH-CHOH-COOK) oldattal. Tartarátot adunk a réz-II-szulfát-oldathoz, hogy stabilizáljuk és megakadályozzuk annak kicsapódását.
CUSO4 + 2 NaOH → Na2CSAK4 + Cu (OH)2
Fehling Reactive (Hermann von Fehling (1812-1885) német vegyészről kapta a nevét)
Fehling reaktív anyagával érintkezve egy aldehid oxidációjával képezi a karbonsavat, míg a rézionok (Cu)2+) közepén található redukálódva vörösesbarna csapadékot képez (téglaszerűbb), amely réz-oxid. A ketonok viszont nem reagálnak - mert nem tudják csökkenteni a Cu ionokat2+.
O O
║ ║
R - C - H + 2 Cu (OH)2 → R ─ C ─ OH + Szamár2O + 2 H2O
aldehid vörösesbarna csapadék
3- Benedek reakciója: Ezt a reaktív anyagot réz-II-szulfát (Cu (OH)2) bázikus közegben, de nátrium-citráttal elegyítjük.
Mint az Fehling-reagens esetében, az aldehid és Benedict-reagens közötti reakció esetében rézionok is vannak (Cu2+) redukált közegben vörös réz-oxidot képeznek.
Ezt a reagenst széles körben használják a vizeletben lévő glükóz jelenlétének és tartalmának kimutatására szolgáló tesztekben. A glükóz szerkezetében aldehidcsoport van, ezért ezekhez a tesztekhez csíkokban lévő Benedict-reagenssel reagál. Innentől kezdve hasonlítsa össze a szalag színét a termék csomagolásán található mérleg színével.

Benedek reagensét használják a vizelet glükóz tartalmának meghatározására.
Írta: Jennifer Fogaça
Kémia szakon végzett
Hivatkozna erre a szövegre egy iskolai vagy tudományos munkában? Néz:
FOGAÇA, Jennifer Rocha Vargas. "Aldehidek és ketonok differenciálása"; Brazil iskola. Elérhető: https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm. Hozzáférés: 2021. június 27.
Kémia

Aldehidek, karbonil-vegyületek, karbonil-csoport, Fő aldehidek, Ethanal, nyersanyag a rovarirtó- és gyógyszeriparban, Metanal, formaldehid-, műanyag- és gyantaipar.
Kémia

Ketonok, szerves anyagok, karbonilcsoport, zománc oldószer előállítása, propanon, ketontestek a véráramban, olajok és zsírok kivonása növényi magokból, oldószerek Organikus.