kemijski element fosfor (P) pripada trećem razdoblju Periodnog sustava i obitelji Azota (VA). Iz tog razloga njegovi atomi obično čine tri kemijske veze doći do teorija okteta (stabilnost). Međutim, postoje neke situacije u kojima atom fosfora stvara više od tri veze, što je činjenica koja je moguća samo putem fenomen hibridizacije.
Da biste razumjeli hibridizacija fosfora, prvo moramo shvatiti zašto atom ovog elementa stvara tri veze. Da bismo to učinili, samo moramo nadzirati vašu elektroničku distribuciju:

Elektronička distribucija fosfora
Možemo primijetiti da u valentnom sloju atom fosfora ima kompletan 3s podrazina (sa dva elektrona) i nepotpuni podrazina 3p (svaka od tri p podnivojske orbitale ima a elektron). Ispod imamo raspodjelu elektrona u orbitalama podnivoa Valentni sloj fosfora:
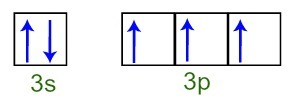
Prikaz elektrona valentne ljuske atoma fosfora
Kako je svaka od 3p orbitala podrazine nepotpuna, atom fosfora je u stanju stvoriti tri kemijske veze, postižući tako stabilnost.
Sada kada pogledamo tvar PCl
5, na primjer, sigurni smo da je u ovoj molekuli fosfor prošao hibridizaciju jer je uspostavio pet veza. Kako klor, koji pripada obitelji VIIA, treba vezu da bi bio stabilan, a molekula ima pet atoma ove element, svaki od njih mora stvoriti vezu, što čini da atom fosfora, zauzvrat, također mora stvoriti pet Veze. Ta je pojava moguća samo putem hibridizacija (spoj nepotpunih atomskih orbitala) fosfora.Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Prilikom primanja energije iz vanjske okoline, elektroni atoma Fosfora pobuđuju se. Ubrzo nakon toga, jedan od dva elektrona koji pripadaju 3s podrazinu pomiče se na praznu orbitalu prisutnu u d podrazinu, koji do tada nema nijedan elektron. Pogledajte donji dijagram:
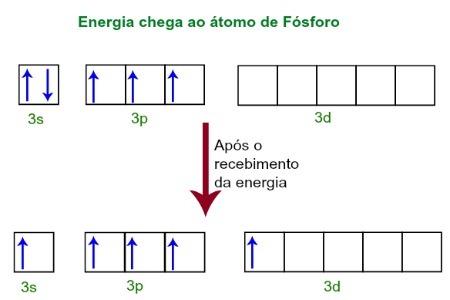
Nakon primanja energije, elektroni fosfora se pobude i jedan zauzima orbitalu podrazine.
U ovom trenutku imamo u valentnom sloju Fosfora s orbitalu, tri p orbitale i nepotpunu d orbitalu.U konačnici se ovih pet orbitala hibridizira, odnosno stapa, što rezultira s pet nepotpunih atomskih orbitala, koje su sada sposobne stvoriti pet kemijskih veza.

Hibridizacija nepotpunih atomskih orbitala fosfora
Kao s orbitala, spojene su tri p orbitale i d orbitala, hibridizacija fosfora je tipa sp3d.
Ja, Diogo Lopes Dias
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
DANI, Diogo Lopes. "Hibridizacija fosfora"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm. Pristupljeno 28. lipnja 2021.
