Prema prvom zakonu termodinamike, u bilo kojem termodinamičkom procesu količina topline P primljen od sustava jednak je radu koji je obavio plus varijaciji njegove unutarnje energije.
Kad je pritisak konstantan, toplina koju sustav izmjenjuje s vanjskim medijem koristi se za rad i za promjenu unutarnje energije. U mnogim praktičnim situacijama sustavi su podvrgnuti atmosferskom tlaku, kao u slučaju kemijske reakcije. Gornja slika prikazuje PV dijagram ove vrste procesa.
U ovom slučaju, u jednadžbi Prvog zakona,
Q = τ + ∆U
niti jedan od pojmova nije nula. Djelo je napisano u funkciji promjene glasnoće volumenaV, kao što su:
τ = P.∆V
Za određeni slučaj idealnog monoatomskog plina, energija se može zapisati kako slijedi:

Stoga možemo napisati Prvi zakon termodinamike u funkciji ΔV:


Toplina izmjenjena s medijem je (5/2) P.ΔV, a 40% od ukupnog broja - što odgovara P.ΔV - koristi se za izvođenje radova; i (3/2) P.ΔV, što odgovara 60% od ukupnog broja, koriste se za izmjenu unutarnje energije. Ovaj rezultat vrijedi za idealan monoatomski plin.
Toplina je povezana s promjenom temperature (koristeći zakon idealnog plina) po:
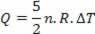
Dakle, isporučena toplina može se izračunati promjenom temperature ili promjenom volumena.
Napisao Domitiano Marques
Diplomirao fiziku
Izvor: Brazil škola - https://brasilescola.uol.com.br/fisica/primeira-lei-para-processos-isobaricos.htm


