Ideje o građi materije (atoma) pojavile su se u staroj Grčkoj, oko 450. pr. a., uglavnom iz Demokrita i Leucipa. Međutim, atom je zapravo dobio znanstveni karakter tek nakon tzv Daltonova atomska teorija.
THE Daltonova atomska teorija bila je temeljna za razvoj atomskog znanja, jer je drugim znanstvenicima poslužila kao osnova za poznavanje atoma i njegovih karakteristika.
Tko je bio John Dalton?
John Dalton, kemičar po struci, rođen je u Cumbriji u Engleskoj 1766. godine, a umro u Manchesteru 1844. godine. Od najranije dobi njegov je život bio predodređen za znanstvena istraživanja i podučavanje, toliko da je predavao ili doprinosio razvoju različitih područja znanja.
Njegovo najveće nasljedstvo kao znanstvenika bio je razvoj prve atomske teorije. Kroz nekoliko eksperimenata povezanih s mješavinom plinova i poznavanjem djela koja je predložio Lavoisier, Daltonova atomska teorija pojavila se 1808. godine.
Postulati Daltonove atomske teorije
Daltonova atomska teorija temeljila se na eksperimentima, ali niti jedan od tih eksperimenata nije mogao jasno otkriti atom. Stoga je Dalton atom nazvao najmanjim dijelom materije.
Daltonova teorija iznosi mnogo više postulata nego dokaza. Pogledajte neke od njih:
Atomi su masivnog i sfernog oblika (slični biljarskoj kugli);
Atomi su nedjeljivi;
Atomi su neuništivi;
Jedan kemijski element to je skup atoma istih svojstava (veličine i mase);
Atomi različitih kemijskih elemenata međusobno se razlikuju;
Relativna težina dvaju atoma može se koristiti za njihovo razlikovanje;
Složena kemikalija nastaje istom kombinacijom različitih vrsta atoma;
Kombinacijom različitih atoma nastaju različite kemijske tvari.
Prikazi Daltonovog atomskog modela
Dalton je svom atomskom modelu dao ime biljarska kugla i, prema tome, počeo je predstavljati atome elemenata poznatih u njegovo doba pomoću sfernih simbola.
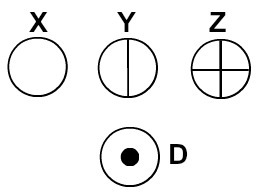
Atomi predstavljeni prema Daltonovoj atomskoj teoriji
Svaki atomski prikaz koji ima određeni detalj ukazuje na drugačiji kemijski element. Didaktički knjige i vježbe osnovne i srednje razine predstavljaju atome samo sferama različitih boja.
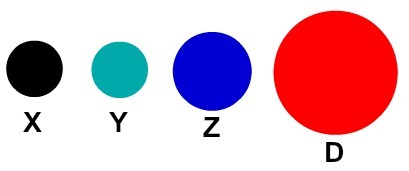
Didaktički prikaz atoma
Prilozi Daltonove atomske teorije
razumijevanje Lavoisierov zakon očuvanja mase
Francuski kemičar Lavoisier tvrdio je 1785. da “U kemijskoj reakciji masa se čuva jer nema ni stvaranja ni uništavanja atoma ”. Daltonova atomska teorija dokazala je tu činjenicu, jer jedan od njegovih postulata kaže da je atom neuništiv.
Stoga, ako izgaramo ugljen (C) u prisutnosti plina kisika (O2), imat ćemo kemijsku reakciju između jednog atoma ugljika i dva atoma kisika. Ova reakcija će stvoriti ugljični dioksid (CO2), koji ima potpuno iste atome koji su tvorili tvari prije reakcije.
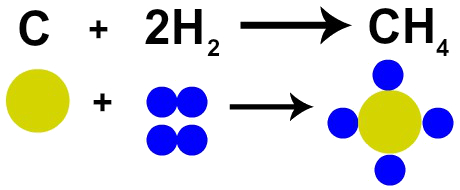
Predstavljanje Lavoisierovog zakona Daltonovim atomskim modelom
razumijevanje jednostavne tvari
Koristiti Daltonov atomski model, možemo razumjeti jednostavnu tvar, odnosno onu koja ima atome iste karakteristike tvoreći molekulu. Stoga imamo atome koji pripadaju istom kemijskom elementu.
U supstanci F2, na primjer, imamo dva atoma fluora, pa u predstavljanju moramo koristiti dvije vrste jednakih atoma prema Daltonovoj atomskoj teoriji.

Jednostavni prikaz supstancije prema Daltonov atomski model
razumijevanje složene tvari
U složenoj tvari imamo atome različitih karakteristika koji tvore molekulu. Stoga imamo različite kemijske elemente koji tvore tvar.
Tvar H2O, na primjer, ima tri atoma: dva vodika i jedan kisik. Pogledajte njegov prikaz prema atomskom modelu Daltona:
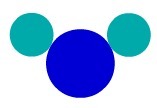
Prikaz složene tvari prema kožiDaltonov atomski model
Razumijevanje smjesa
Razumijevanje smjese (sjedinjavanje dviju ili više različitih tvari) kroz Daltonovu atomsku teoriju jednostavno je: samo stavite dvije različite molekule u isti spremnik.

Prikaz druge smjese Daltonov atomski model
Ostali znanstveni prilozi Johna Daltona
uveo koncept atomska masa;
Oblikovao zakon parcijalnih pritisaka plinova (Daltonov zakon);
Otkrio oštećenje vida tzv daltonizam;
Proučavao ponašanje para i plinova pri različitim temperaturama;
Otkrio je da se svi plinovi na isti način šire (pokušavaju zauzeti određeno mjesto) u prostoru.
Ja, Diogo Lopes Dias
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/teoria-atomica-dalton.htm
