Jedan reakcija energetske oksidacije u alkenima nastaje kad dođe do puknuća molekule, odnosno istodobnog prekida dviju dvostrukih veza i ulaz kisika u organskoj molekuli.
Ovu vrstu reakcije moguće je provesti s alkenima kada se koristi kalijev permanganat (KMnO4) ili kalijev dikromat (K2Cr2O7) koncentrirano, u kiselom mediju, dok je vruće.
U kiselom mediju nalaze se ioni H3O+ uzrokujući raspadanje KMnO4 i oslobađanje 5 atoma novonastalog kisika [O] za svaka 2 KMnO4. Primijetite ovu razgradnju u nastavku:

Ova se reakcija naziva "energetskom" jer razbija dvije veze dvojnika (u blagoj oksidaciji samo je veza prekinuta pi), drugi je čimbenik da je to smanjenje mangana u kiselom mediju mnogo intenzivnije nego u baznom mediju, kao što se to radi u blaga oksidacija.
Otpušteni kisik koji reagira tada reagira s alkenom, ali konačni proizvod ovisi o tome koji je vrste ugljika koje povezuju dvostruku vezu, tj. ako su primarne, sekundarne ili tercijarni. Pogledajte što se događa u svakom slučaju:
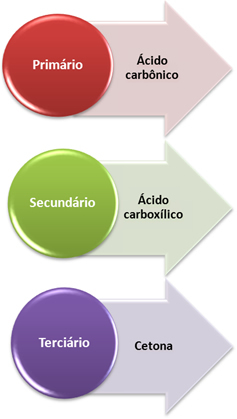
- Primarni ugljik: Ako je nezasićenje između dva primarna ugljika, nastali proizvodi će biti dva ugljične kiseline (H2CO3). Ako je samo jedan od ugljika u dvostrukoj vezi primarni, samo će jedna od formiranih molekula biti ugljična kiselina. Međutim, ovaj je spoj nestabilan i nikada nije izoliran, već se raspada voda i ugljični dioksid.
- Sekundarni ugljik: Ako je nezasićenje između dva sekundarna ugljika, nastat će dva produkta karboksilne kiseline. Ako je samo jedan od ugljika sekundarni, nastat će molekula karboksilne kiseline, dok će drugi ovisiti o drugom ugljiku.
- Tercijarni ugljik: Rađa keton.
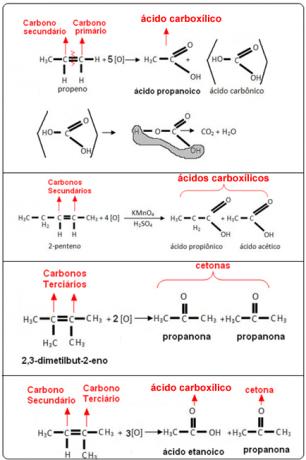
Pogledajte primjere u nastavku:
Napisala Jennifer Fogaça
Diplomirao kemiju
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcenos.htm


