imamo miješanje otopina s različitim otopljenim tvarima bez kemijske reakcije kada dvije ili više smjesa kojima su zajedničke tvari s istim ionom (ili isti kation ili isti anion). Kao u primjeru u nastavku:
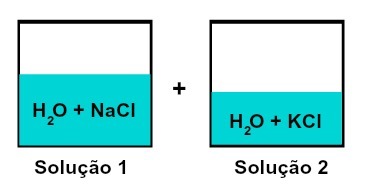
Smjesa otopina koje imaju različite otopljene tvari
Otopina 1 je voda i natrijev klorid (NaCl), dok otopina 2 sadrži vodu i kalijev klorid (KCl). Kad se pomiješaju, imamo a miješanje različitih otopljenih otopljenih tvari bez kemijske reakcije, jer obje korištene soli imaju kloridni anion (Cl-).
1- Karakteristike smjesa različitih otopina otopljenih tvari bez kemijske reakcije
Kad se provodi mješavina otopina koje imaju različite otopljene tvari bez kemijske reakcije, uvijek se provjeravaju donje karakteristike:
Masa svake otopljene tvari se ne mijenja (ako u otopini 1 imamo 10 g otopljene tvari, a u 2, 30 g, na primjer, nakon miješanja imat ćemo istu masu svake otopljene tvari),
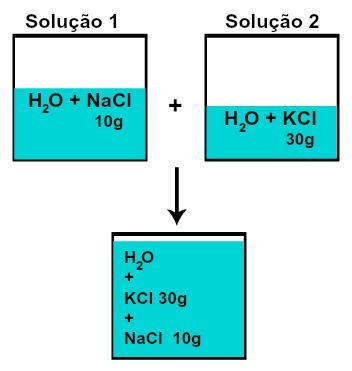
Masa svake otopljene tvari nakon miješanja otopina bez kemijske reakcije
THE količina materije (n) svake se otopljene tvari ne mijenja (ako u otopini 1 imamo 5 mola otopljene tvari, a u 2, 4 mola, na primjer, nakon miješanja imat ćemo istu količinu materije svake od njih),
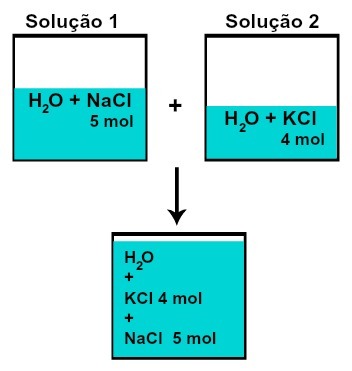
Broj molova svake otopljene tvari nakon miješanja otopina bez kemijske reakcije
Volumen konačnog rješenja, VF, rezultat je zbroja volumena svake od pomiješanih otopina (ako u otopini 1 imamo 200 ml, a u otopini 2, 300 ml, na primjer, nakon miješanja imat ćemo 500 ml volumena),
VF = V1 + V2
2- Formule korištene u proračunima miješanja otopina različitih otopljenih tvari bez kemijske reakcije.
Kao što kod ove vrste smjese imamo samo porast količine otapala u odnosu na svaki od otopljene tvari, moramo izračunati konačnu koncentraciju svake od otopljenih tvari koristeći sljedeće izrazi:
a) Za zajednička koncentracija (Ç)
Za otopinu 1: množenje koncentracije otopine 1 s njezinim volumenom jednako je konačnoj koncentraciji pomnoženoj s njezinim volumenom
Ç1.V1 = CF.VF
Za otopinu 2: množenje koncentracije otopine 2 s njezinim volumenom jednako je konačnoj koncentraciji pomnoženoj s njezinim volumenom
Ç2.V2 = CF.VF
b) Za koncentracija u količini materije ili molarnost (M)
Za rješenje 1:
M1.V1 = MF.VF
Za rješenje 2:
M2.V2 = MF.VF
c) Koncentracija u količini materije svakog iona prisutnog u otopini
Ako moramo odrediti koncentraciju jednog ili svih iona prisutnih u konačnoj otopini, moramo:
1º: Zapamtite da se koncentracija iona daje množenjem koncentracije (M) otopljene tvari iz koje dolazi, njezinim indeksom u formuli supstance. Dakle, za ion Y, u supstanci 1, XY3, koncentracija će biti:
[Y]1 = 3. M
Što se tiče otopljene tvari2, ZY, koncentracija Y bila bi dana:
[Y]2 = 1. M
2º: Ako imamo više otopljenih tvari koje oslobađaju isti ion, na primjer, otopljene tvari XY3 i ZY, koji imaju isti ion Y, koncentracija ovog iona u konačnoj otopini daje se zbrojem njegovih koncentracija za svaku otopljenu supstancu:
[Y]F = [Y]1 + [Y]2
3- Primjeri izračuna koji uključuju miješanje otopina različitih otopljenih tvari bez kemijske reakcije
Primjer 1: (PUC SP) U čaši je pomiješano 200 ml vodene otopine kalcijevog klorida (CaCl)2) od 0,5 mol koncentracije. L–1 i 300 ml 0,8 mol otopine. L–1 natrijevog klorida (NaCl). Dobivena otopina ima koncentraciju kloridnog aniona približno:
a) 0,34 mol. L–1
b) 0,65 mol. L–1
c) 0,68 mol. L–1
d) 0,88 mol. L–1
e) 1,3 mol. L–1
Podaci dobiveni vježbom bili su:
Rješenje 1:
Svezak (V1): 200 ml
Molarna koncentracija (M1): 0,5 mol. L–1
Rješenje 2:
Svezak (V2): 300 ml
Molarna koncentracija (M2): 0,8 mol. L–1
Za određivanje koncentracije kloridnih aniona (Cl-), moramo slijediti ove korake:
Korak 1: izračunati volumen konačnog rješenja
VF = V1 + V2
VF = 200 + 300
VF = 500 ml
Korak 2: Izračunati molarnu koncentraciju konačne otopine s obzirom na otopinu CaCl2, koristeći izraz u nastavku:
M1.V1 = MF.VF
0,5,200 = MF.500
100 = MF.500
100 = MF
500
MF = 0,2 mol. L–1
Korak 3: Izračunati molarnu koncentraciju klorida [Cl-]1, u konačnoj otopini, iz otopljene tvari CaCl2, koristeći izraz u nastavku:
BILJEŠKA: U formuli imamo množenje molarnosti s 2, jer imamo indeks 2 u Cl, u formuli otopljene tvari CaCl2.
[Kl-]1 = 2.MF
[Kl-]1 = 2. 0,2
[Kl-]1 = 0,4 mol. L–1
Korak 4: Izračunajte molarnu koncentraciju konačne otopine s obzirom na otopljenu NaCl, koristeći sljedeći izraz:
M2.V2 = MF.VF
0,8 300 = MF.500
240 = MF.500
240 = MF
500
MF = 0,48 mol. L–1
Korak 5: Izračunati molarnu koncentraciju klorida, [Cl-]2, u konačnoj otopini, iz otopljene otopine NaCl, koristeći donji izraz:
BILJEŠKA: U formuli imamo množenje molarnosti s 1, jer imamo indeks 1 u Cl, u formuli za otopljenu NaCl.
[Kl-]2 = 1.MF
[Kl-]2 = 1. 0,48
[Kl-]2 = 0,48 mol. L–1
Korak 6: Izračunajte ukupnu količinu kloridnih iona u konačnoj otopini
Da biste to učinili, samo dodajte molarne koncentracije klorida za svaku od otopljenih tvari u koracima 3 i 5:
[Kl-]F = [Kl-]1+ [Kl-]2
[Kl-]F = 0,4 + 0,48
[Kl-]F = 0,88 mol. L–1
Primjer 2: Otopini od 500 ml 6 mol / L KOH doda se 300 ml otopine K.2SAMO3 3 mol / L. Kolika je koncentracija svake od otopljenih tvari u dobivenoj smjesi
a) 3,75 i 3,0 mol / L
b) 3,75 i 1,225 mol / L
c) 4,5 i 1,125 mol / L
d) 3,75 i 1,125 mol / L
e) 4,5 i 1,251 mol / L
Podaci dobiveni vježbom bili su:
Rješenje 1:
Svezak (V1): 500 ml
Molarna koncentracija (M1): 6 mol. L–1
Rješenje 2:
Svezak (V2): 300 ml
Molarna koncentracija (M2): 3 mol. L–1
Za određivanje koncentracije kloridnih aniona (Cl-), moramo slijediti ove korake:
Korak 1: izračunati volumen konačnog rješenja
VF = V1 + V2
VF = 500 + 300
VF = 800 ml
Korak 2: Izračunajte molarnu koncentraciju konačne otopine s obzirom na otopinu KOH, koristeći sljedeći izraz:
M1.V1 = MF.VF
6.500 = MF.800
3000 = MF.800
3000 = MF
800
MF = 3,75 mol. L–1
Korak 3: Izračunati molarnu koncentraciju konačne otopine u odnosu na otopljenu supstancu K2SAMO3, koristeći izraz u nastavku:
M2.V2 = MF.VF
3.300 = MF.800
900 = MF.800
900 = MF
800
MF = 1,125 mol. L–1
Ja, Diogo Lopes Dias
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/mistura-solucoes-com-solutos-diferentes-sem-reacao-quimica.htm

