Disocijacija baze to je fizički proces koji se događa s ovom važnom skupinom anorganskih tvari kada se otope u vodi, ili kada prolaze kroz proces fuzije (prelazak iz krutog u tekuće stanje kroz grijanje).
Općenito, fenomen disocijacija baze to je oslobađanje kationa i aniona koji tvore ionski spoj, koja je, u ovom slučaju, baza. Dakle, tijekom disocijacija baze, puštanje ioni koji već postoje u spoju, odnosno ne stvaraju se novi ioni.
Bazu tvori bilo koji metal (X), koji je kation spoja, ili amonijev kation (NH skupina4+), vezan za hidroksid anion (predstavljen OH skupinom), kao u prikazima u nastavku:
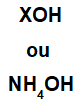
Opći prikazi osnovne formule
oblik predstavljaju disocijacija baze to se vrši kroz jednadžbu u kojoj u reaktantu imamo bazu, a u produktima ione (katione i anione). Ono što čini razliku je kako se odvija disocijacija:
Otapanje baze u vodi:
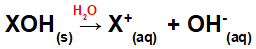
Jednadžba koja predstavlja disocijaciju baze u vodenom mediju
Disocijacija osnovnim spajanjem:
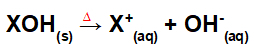
Jednadžba koja predstavlja disocijaciju baze postupkom fuzije
Analizirajući gornje opće jednadžbe, provjeravamo da ćemo u svima njima uvijek imati bazu, kation (a to je metal ili NH skupina
4+) i anion (OH-). Ali jesu li svi takvi? Nema li razlike među njima? Na prvo pitanje odgovor je ne, a na drugo pitanje da.Kada provodimo disocijacija od baze, prvo je bitno analizirati osnovnu formulu, jer iz nje možemo odrediti opterećenje kation i mol količina hidroksidnih aniona, budući da je molska količina kationa standardna (uvijek 1 mol).
Vrijedno je podsjetiti da količina OH skupina prisutnih u bazičnoj formuli određuje naboj kationa i količinu hidroloksidnog aniona u disocijaciji baze.
Pogledajmo primjere aluminij hidroksida [Al (OH)3] i zlatni hidroksid (AuOH). U osnovnoj formuli aluminija postoje tri OH skupine, a u zlatnoj bazi samo jedna OH skupina. Dakle, u disocijaciji ovih baza imamo:
Al (OH) disocijacija3:
Kako ova baza ima tri OH skupine u formuli, naboj na kationu bit će +3, a količina u molima aniona jednaka je 3 mola, kao što možemo vidjeti u sljedećoj jednadžbi:
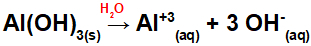
Jednadžba disocijacije baze aluminija u vodenom mediju
Disocijacija od AuOH:
Kako ova baza ima OH skupinu u formuli, naboj na kationu bit će +1, a količina u molima aniona jednaka je 1 molu, kao što možemo vidjeti u sljedećoj jednadžbi:
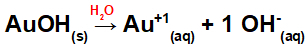
Jednadžba disocijacije baze sa zlatom u vodenom mediju
Ja, Diogo Lopes Dias
Izvor: Brazil škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm