Jedan reakcija dodavanja je kemijski postupak u kojem se organskoj molekuli dodaju atomi anorganske tvari koja mora imati jednu od sljedećih karakteristika:
Otvorena struktura koja sadrži vezivanje ili pi veze;
Zasićena zatvorena struktura (samo sa sigma veze);
Zatvorena nezasićena struktura (s pi ili aromatskom vezom).
Organski spojevi koji imaju ove karakteristike su sljedeći Ugljikovodici:
alkeni;
Alkini;
Alkadienes;
Ciklani;
Ciklusi;
Aromatika.
Tijekom a reakcija dodavanja, jedna ili više pi veza ili sigma veza (u isključivom slučaju ciklana) su prekinute uzrokujući pojavljivanje dvije ili više slobodnih valencija (mjesta vezivanja) na zahvaćenim ugljicima, kao u primjeru dolje:
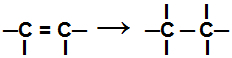
Prekidanje veze pi u alkenu
Nakon što se ta veza prekine, dodavanje atoma mora se dogoditi na novim mjestima vezivanja stvorenim u organskom spoju. U nastavku navodimo vrste reakcije zbrajanja koji se mogu provesti s organskim spojevima.
hidrogeniranje
U ovome reakcija dodavanja, osim organskog spoja, drugi reaktant je plinoviti vodik (H
2). U svakom od ugljika, gdje se događa fisija (prekid sigme ili pi veze, kao što se vidjelo prije), bit će veza atoma vodika koja se odnosi na količinu prekinutih veza.Na primjer, kada provodimo hidrogeniranje ciklobutana, između ugljika 1 i 2 prekida se sigma veza. Zatim se atom vodika veže za svaki od ovih ugljika:
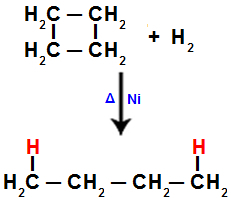
Jednadžba koja predstavlja hidrogeniranje u ciklobutanu
Halogenizacija
Pored organskog spoja, drugi reagens u tome reakcija dodavanja je molekularni halogen (klor-Cl plin2, fluor-F plin2, čvrsti jod-I2 i tekući brom-Br2). Na svakom ugljiku, gdje se događa fisija (prekid sigme ili pi veze, kao što se vidi gore), bit će veza atoma halogen koji se odnosi na broj prekinutih veza.
Dakle, kada provodimo halogeniranje (pomoću plina klora) ciklopropena, pi veza se prekida između ugljika 1 i 2. Zatim se atom klora veže za svaki od ovih ugljika:

Jednadžba koja predstavlja halogeniranje u ciklopropenu
Reakcija adicije s halidom
Halogenid je anorganska hidra kiselina, koju tvore atom vodika i atom vodika. halogen, kao što je klorovodična kiselina (HCl), fluorovodična kiselina (HF), bromovodična kiselina (HBr), kiselina hidrojodni (HI).
Na reakcija dodavanja s halidom, uz organski spoj, drugi reagens je halid, dakle jedan od ugljika, gdje cijepljenje (prekid sigme ili pi veze, kao što se vidi gore), mora primiti atom vodika, a drugi prima halogenida.
Prema Vladavina Markovnikova, hidrogenirani ugljikov atom (ili ugljik vezan za manji radikal) mora primiti vodik, a manje hidrogenirani ugljik (ili ugljik vezan za veći radikal) mora primiti halogenida.
Na primjer, kada ovu reakciju izvodimo na propenu s klorovodičnom kiselinom (HCl), pi veza se prekida između ugljika 1 i 2. Zatim se vodik veže na ugljik 1 (više hidrogeniran), a klor na ugljik 2 (manje hidrogeniran):
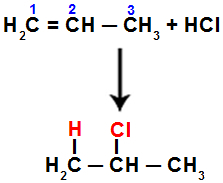
Jednadžba koja predstavlja dodatak halogenidu u propenu
Reakcija hidratacije
Kad ionizira molekula vode, stvara se hidronijev kation (H+) i hidroksid anion (OH-). Iz tog razloga, u ovom reakcija dodavanja, osim organskog spoja, drugi reaktant je voda. Dakle, jedan od ugljika, gdje dolazi do cijepanja (razbijanje sigme ili pi veze, kao što se vidi gore), prima kation hidronija, a drugi hidroion-anion.
Prema pravilu Markovnikova, najviše hidrogenirani atom ugljika (ili ugljik vezan za manji radikal) mora primiti hidronij, a manje hidrogenizirani ugljik (ili ugljik vezan za veći radikal) mora dobiti hidroksid.
Na primjer, kada hidratiziramo penta-1,4-diene, pi veza se prekida između ugljika 1 i 2 te između ugljika 4 i 5. Tada ugljik 1 i 5 primaju hidronij, a ugljik 2 i 4 hidroksid:
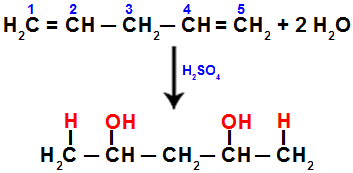
Jednadžba koja predstavlja dodatak s hidratacijom u penta-1,4 dienu
Ja, Diogo Lopes Dias
Izvor: Brazil škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-reacao-adicao.htm