Među međumolekularnim silama, inducirane dipolom inducirane dipolne sile oni su jedini koje nije proučavao nizozemski fizičar Johannes Diederik Van der Waals (1837-1923). Njih je rasvijetlio njemački fizičar Fritz Wolfgang London (1900.-1954.), pa se te sile nazivaju i londonske snage ili londonske disperzijske snage. Drugi naziv za ove sile je trenutni dipolom inducirani dipol.
Ova vrsta sile javlja se u nepolarne tvari, kao što su H2, O2, F2, Cl2, CO2, CH4 i C2H6, između ostalih. A mogu se pojaviti i između atoma plemenitog plina, kada se približe, uzrokujući odbojnost između njihovih elektrosfera. Na taj način se elektroni akumuliraju na određenoj strani koja je negativno polarizirana, a suprotna pozitivno, zbog nedostatka negativnog naboja.
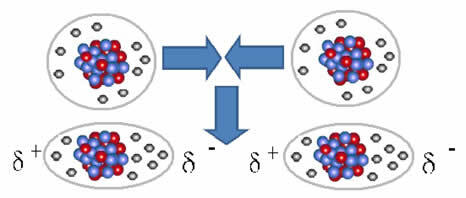
Nepolarne molekule mogu prijeći iz plinovitog stanja – u kojem su vrlo udaljene jedna od druge i nema interakcije, jer nema polova – u tekuće i čvrsto stanje. U tim stanjima agregacije, molekule su bliže i elektroničko privlačenje ili odbijanje između njihovih elektrona i jezgre mogu dovesti do deformacije njihovih elektronskih oblaka, trenutno, stvarajući pozitivne i negativne polove privremeni.
Trenutačni dipoli mogu izazvati polarizaciju susjednih molekula, što rezultira privlačnim silama.
Ova indukcija se također može dogoditi. između različitih molekula i općenito te su sile slabijeg intenziteta od jačine dipol-dipola i vodikove veze. Stoga su krute tvari s ovom snagom interakcije kao što su suhi led (ugljični dioksid – CO2) i jod (I2), koji su u čvrstom stanju, sublimne (prelaze u plinovito stanje); jer je energija potrebna da se poremete njihove interakcije mala.
Primjer međumolekularnih sila između polarnih i nepolarnih molekula javlja se između plina kisika (nepolarnog) i vode (polarnog). Ispada da se negativni kraj vode približava O2, odbijajući se, pa se tako elektronski oblak nepolarne molekule udaljava. Kisik se tada trenutno polarizira i počinje komunicirati s vodom, otapajući se u njoj.
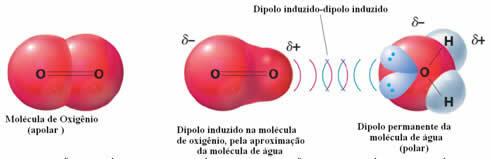
Budući da su te sile slabe, topljivost ovog plina u vodi je mala. Unatoč tome, njegova prisutnost je neophodna za očuvanje života raznih vodenih organizama.
Ova sila interakcije također se javlja u prirodi, osiguravajući prianjanje između šapa gekona i površine po kojoj hodaju. Zato mogu hodati po zidovima i stropovima bez pada ili zalijepljenosti.
Autora Jennifer Fogaça
Diplomirao kemiju
Školski tim Brazila
Izvor: Brazil škola - https://brasilescola.uol.com.br/quimica/forcas-dipolo-induzido-dipolo-induzido-ou-dispersao-london.htm
