Kiselinski oksidi su oni oksidi koji u reakciji s vodom stvaraju kiselinu kao proizvod. Kad reagiraju s bazom, proizvodi će biti sol i voda.
Ti spojevi obično imaju kovalentni karakter, odnosno molekularni su, topljivi su u vodi i nastaju uglavnom od nemetala, koji su elementi s velikom elektronegativnošću. Kada ih tvore metali, oni imaju visoke oksidacijske brojeve (električni naboj).
Primjeri:
CO2, SAMO2, SAMO3, Str2O5, Cl2O6, NA2, ne2O4, ne2O5itd.
Slijedi općenita shema karakterističnih reakcija za kisele okside i primjer:
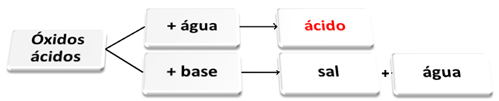
Kiselinski oksidi koji reagiraju s vodom i s bazom
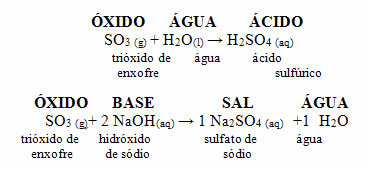
Zovu se i kiselinski oksidi anhidridi, jer ova riječ dolazi iz grčkog anhidros, što znači "nema vode", a kiseli oksidi mogu se smatrati „kiselinom bez vode“.
Svojstva i primjena nekih kiselih oksida:
• Ugljični dioksid (ugljični dioksid) - CO2:
Ovaj se spoj koristi kao plin u bezalkoholnim pićima i u mineralnim vodama, jer kada je podvrgnut visokom tlaku, postaje topiv u vodi. U tim proizvodima stvara kiseli medij, jer je kiseli oksid koji reagira s vodom, stvarajući kiselinu, prema reakciji dolje:

Ispod 78 ° C nalazi se u čvrstom stanju i poznat je pod nazivom suhi led, koji je ime dobio jer izgledom podsjeća na led. uobičajena, ali se ne topi, prelazeći u tekuće stanje na sobnoj temperaturi, već prelazi u parno stanje, odnosno sublimira. Stoga se ova značajka koristi kao scenski resurs u koncertima, filmovima, kazalištima, zabavama itd.

Ugljični dioksid je kiseli oksid
Također se nalazi u atmosferi kao rezultat ljudskog disanja, izgaranja fosilnih goriva (ugljen, naftni derivati, alkohol itd.) I šumskih požara. Dakle, jedan je od odgovornih za kisele kiše.
• Sumporni oksidi - SO2 i tako3
Ti su oksidi također prisutni u atmosferi, jer su prirodnog i umjetnog podrijetla. Prirodno se događa vulkanskim erupcijama i razgradnjom biljaka i životinja. Umjetno odgovara najvećoj količini ovih oksida u atmosferi, kakvi jesu izbačeni izgaranjem fosilnih goriva, uglavnom dizelskog ulja, koje sadrži sumpor kao što je nečistoća.
Sumpor-dioksid (SO2) reagira s kisikom iz atmosfere stvarajući sumporni trioksid (SO3). Kada ovaj posljednji oksid reagira s kišnicom, nastaje sumporna kiselina koja je vrlo jaka i uzrokuje štetu.
• Izgaranje sumpora iz goriva: S + O2 → OS2
• Transformacija SO2 u SO3: SO2 + ½2 → OS3
Reakcije SO2 i SO3 s vodom dajući kiseline: SO2 + H2O → H2SAMO3
SAMO3 + H2O → H2SAMO4
• Dinitrogen tetroksidi (nitrat-dušikov anhidrid) - N2O4
Ovaj spoj ima tačku vrenja 22 ° C, ima žutu boju i prilično je hlapljiv. Nastaje u atmosferi oksidacijom dušika i može biti u tekućem obliku, u obliku dimera mononitrogen dioksida ili dušikovog oksida (NO2). Iznad te temperature poprima oblik NO2:
N2O4 ↔ NE2
To je izuzetno otrovni plin i njegovo udisanje je kobno. Također se koristi u sastavu raketnih goriva.
Napisala Jennifer Fogaça
Diplomirao kemiju

